在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述正确的是( )
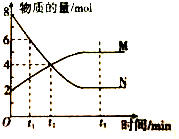

| A、反应的化学方程式:2N?M |
| B、t2时,正、逆反应速率相等,达到平衡 |
| C、t3时,正反应速率大于逆反应速率 |
| D、反应开始时只投入了N |
在一定条件下,可逆反应X(g)+3Y(g)=2Z(g) 达到反应限度时,有25%的X转化为Z,有37.5%的Y转化为Z,则开始时充入容器中的X和Y的物质的量之比为( )
| A、1:2 | B、2:1 |
| C、1:3 | D、3:1 |
一定条件下,在体积为2L的密闭容器中,3molX和3mol Y发生反应:3X(g)+Y(g)═2Z(g),经60s达到平衡,生成0.4molZ.下列说法正确的是( )
| A、60s内反应速率为v(X)=0.05 mol/(L?s),X的转化率为80% | ||
B、其它条件不变,将容器体积变为4L,Z的平衡浓度变为原来的
| ||
| C、其它条件不变,若升高温度,X的体积分数增大,则该反应的△H>0 | ||
| D、其它条件不变,若初始投入2mol X和2mol Y则物质Y的转化率减小 |
 某温度时,有5L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示,根据图中数据填空
某温度时,有5L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示,根据图中数据填空 纯碱、烧碱等是重要的化工原料.
纯碱、烧碱等是重要的化工原料.