题目内容
A→G均为有机化合物,其中A为二卤代烃,相对分子质量为216,碳的质量分数为22.2%;一个B分子中含6个H;相关转化关系如下:
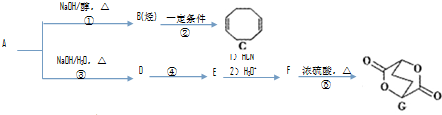
已知:
请回答:
(1)E中官能团名称为 ;G的分子式为 .
(2)④的反应类型为 .
(3)下列关于F的说法正确的是 (填选项字母).
a.1mol F与足量金属钠反应最多生成4mol H2
b.1mol F完全燃烧消耗8.5mol O2
c.能与新制Cu(OH)2悬浊液反应生成砖红色沉淀
d.能与NaHCO3反应生成CO2
(4)写出下列反应的化学方程式:反应③ ;反应⑤ .
(5)与E互为同系物并且相对分子质量比E大14的同分异构体有 种,其中核磁共振氢谱中有2个吸收峰并且峰面积之比为3:1的分子的结构简式为 .

已知:

请回答:
(1)E中官能团名称为
(2)④的反应类型为
(3)下列关于F的说法正确的是
a.1mol F与足量金属钠反应最多生成4mol H2
b.1mol F完全燃烧消耗8.5mol O2
c.能与新制Cu(OH)2悬浊液反应生成砖红色沉淀
d.能与NaHCO3反应生成CO2
(4)写出下列反应的化学方程式:反应③
(5)与E互为同系物并且相对分子质量比E大14的同分异构体有
考点:有机物的推断
专题:有机物的化学性质及推断
分析:A为二卤代烃,相对分子质量为216,碳的质量分数为22.2%,则A中的碳原子数为
=4,根据A→B→C的变化,及C的结构简式可知,B为1,4-丁二烯,A的分子式可写为C4H8X2,则X的相对原子质量为80,X为Br.根据G的结构,可推知F的结构为 ,根据已知信息,可知E为OHC-CH2-CH2-CHO,则逆推可知D为HOCH2CH2CH2CH2OH,则A为BrCH2CH2CH2CH2Br,据此解答.
,根据已知信息,可知E为OHC-CH2-CH2-CHO,则逆推可知D为HOCH2CH2CH2CH2OH,则A为BrCH2CH2CH2CH2Br,据此解答.
| 216×22.2% |
| 12 |
 ,根据已知信息,可知E为OHC-CH2-CH2-CHO,则逆推可知D为HOCH2CH2CH2CH2OH,则A为BrCH2CH2CH2CH2Br,据此解答.
,根据已知信息,可知E为OHC-CH2-CH2-CHO,则逆推可知D为HOCH2CH2CH2CH2OH,则A为BrCH2CH2CH2CH2Br,据此解答.解答:
解:A为二卤代烃,相对分子质量为216,碳的质量分数为22.2%,则A中的碳原子数为
=4,根据A→B→C的变化,及C的结构简式可知,B为1,4-丁二烯,A的分子式可写为C4H8X2,则X的相对原子质量为80,X为Br.根据G的结构,可推知F的结构为 ,根据已知信息,可知E为OHC-CH2-CH2-CHO,则逆推可知D为HOCH2CH2CH2CH2OH,则A为BrCH2CH2CH2CH2Br,
,根据已知信息,可知E为OHC-CH2-CH2-CHO,则逆推可知D为HOCH2CH2CH2CH2OH,则A为BrCH2CH2CH2CH2Br,
(1)由上述分析可知,E为OHC-CH2-CH2-CHO,含有官能团为:醛基,由G的结构可知其分子式为C6H6O4,故答案为:醛基;C6H6O4;
(2)反应④D→E是醇被氧化生成醛,属于氧化反应,故答案为:氧化反应;
(3)F的结构简式为 ,
,
a.分子中的羟基、羧基均可与Na反应,因此1molF与Na反应可生成2mol H2,故a正确;
b.F的分子式为C6H10O6,1molF燃烧的耗氧量为(6+
-
)mol=5.5mol,故b错误;
c.F中不含醛基,不能与新制Cu(OH)2反应,故c错误;
d.F中的羧基可与NaHCO3反应生成CO2,故d正确,
故选:ad;
(4)反应③为卤代烃水解产生醇,反应方程式为:BrCH2CH2CH2CH2Br+2NaOH
HOCH2CH2CH2CH2OH+2NaBr,
反应⑤为醇、羧酸的酯化,反应方程式为:
 +2H2O,
+2H2O,
故答案为:BrCH2CH2CH2CH2Br+2NaOH
HOCH2CH2CH2CH2OH+2NaBr;

 +2H2O;
+2H2O;
(5)与E(OHC-CH2-CH2-CHO)互为同系物,则含有的官能团种类、数目相同,相对分子质量比E大14,则分子式比E多CH2,符合条件的同分异构体有:OHCCH2CH2CH2CHO、CH3CH2CH(CHO)2、CH3CH(CHO)CH2CHO、CH3C(CHO)2CH3,共有4种,其中核磁共振氢谱中有2个吸收峰并且峰面积之比为3:1的分子的结构简式为 CH3C(CHO)2CH3,故答案为:4; CH3C(CHO)2CH3.
| 216×22.2% |
| 12 |
 ,根据已知信息,可知E为OHC-CH2-CH2-CHO,则逆推可知D为HOCH2CH2CH2CH2OH,则A为BrCH2CH2CH2CH2Br,
,根据已知信息,可知E为OHC-CH2-CH2-CHO,则逆推可知D为HOCH2CH2CH2CH2OH,则A为BrCH2CH2CH2CH2Br,(1)由上述分析可知,E为OHC-CH2-CH2-CHO,含有官能团为:醛基,由G的结构可知其分子式为C6H6O4,故答案为:醛基;C6H6O4;
(2)反应④D→E是醇被氧化生成醛,属于氧化反应,故答案为:氧化反应;
(3)F的结构简式为
 ,
,a.分子中的羟基、羧基均可与Na反应,因此1molF与Na反应可生成2mol H2,故a正确;
b.F的分子式为C6H10O6,1molF燃烧的耗氧量为(6+
| 10 |
| 4 |
| 6 |
| 2 |
c.F中不含醛基,不能与新制Cu(OH)2反应,故c错误;
d.F中的羧基可与NaHCO3反应生成CO2,故d正确,
故选:ad;
(4)反应③为卤代烃水解产生醇,反应方程式为:BrCH2CH2CH2CH2Br+2NaOH
| H2O |
| △ |
反应⑤为醇、羧酸的酯化,反应方程式为:

| 浓硫酸 |
| △ |
 +2H2O,
+2H2O,故答案为:BrCH2CH2CH2CH2Br+2NaOH
| H2O |
| △ |

| 浓硫酸 |
| △ |
 +2H2O;
+2H2O;(5)与E(OHC-CH2-CH2-CHO)互为同系物,则含有的官能团种类、数目相同,相对分子质量比E大14,则分子式比E多CH2,符合条件的同分异构体有:OHCCH2CH2CH2CHO、CH3CH2CH(CHO)2、CH3CH(CHO)CH2CHO、CH3C(CHO)2CH3,共有4种,其中核磁共振氢谱中有2个吸收峰并且峰面积之比为3:1的分子的结构简式为 CH3C(CHO)2CH3,故答案为:4; CH3C(CHO)2CH3.
点评:本题考查有机物推断、官能团、有机物结构与性质、同分异构体等,注意根据有机物的结构与反应信息,利用逆推法进行推断,需要学生具备扎实的基础与一定推理能力,难度中等.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
下列关于氯水的叙述,正确的是( )
| A、新制氯水中只含Cl2和H2O分子 |
| B、新制氯水可使蓝色石蕊试纸先变红后褪色 |
| C、光照氯水有气泡逸出,该气体是Cl2 |
| D、氯水放置数天后酸性会减小 |
下列有关实验的说法错误的是( )
| A、做银镜反应实验后的试管内壁附有银,可用稀硝酸清洗 |
| B、向MgCl2溶液中滴加NaOH溶液,产生白色沉淀,再加入FeCl3溶液,沉淀逐渐变为红褐色 |
| C、用0.1mol/L的酸性KMnO4溶液配成的溶液滴定一定质量的草酸晶体(H2C2O4?nH2O)以测定其n值,若终点仰视读数,则n值偏大 |
| D、环形玻璃搅拌棒材料若用铜代替,则测量出的中和热数值偏小 |
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述正确的是( )
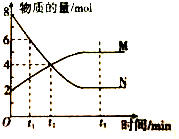

| A、反应的化学方程式:2N?M |
| B、t2时,正、逆反应速率相等,达到平衡 |
| C、t3时,正反应速率大于逆反应速率 |
| D、反应开始时只投入了N |
短周期元素X、Y、Z在周期表中的相对位置如图所示,下列判断正确的是( )
| X | ||
| Y | ||
| Z |
| A、X是最活泼的非金属元素 |
| B、Y的最高化合价为+7 |
| C、Z原子的最外层电子数是6 |
| D、3种元素的单质分子都是双原子分子 |

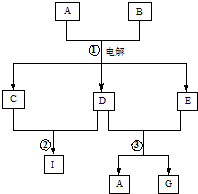 在如图所示的物质转化关系中,A是海水中含量最丰富的盐,B是常见的无色液体,G的水溶液是一种常用的漂白剂.(反应中生成的水和部分反应条件未列出)
在如图所示的物质转化关系中,A是海水中含量最丰富的盐,B是常见的无色液体,G的水溶液是一种常用的漂白剂.(反应中生成的水和部分反应条件未列出)