下列分离、提纯、鉴别物质的方法正确的是( )
| A、用过滤的方法除去NaCl溶液中含有的少量淀粉胶体 |
| B、用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 |
| C、用加热、蒸发的方法可以除去粗盐中的CaCl2、MgCl2等杂质 |
| D、用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液 |
下列有关实验的说法不正确的是( )
| A、当沉淀的颗粒较大时,也可用倾析法将固体和溶液分离 |
| B、结晶时,若溶质的溶解度越小,或溶液的浓度越高、或溶剂的蒸发速度越快,析出的晶粒就越细小 |
| C、硫酸亚铁铵晶体过滤后用无水乙醇洗涤而不要用水洗涤主要是为了减少晶体损失 |
| D、阿司匹林制备实验中,将粗产品加入饱和NaOH溶液中以除去水杨酸聚合物 |
将10.416克纯铁丝溶于过量的盐酸中,在加热条件下,用5.05克的KNO3去氧化溶液中的Fe2+,待反应完全后,剩余Fe2+还需要24ml0.3mol/L的KMnO4溶液才能完全氧化成Fe3+,此时MnO4-转化为Mn2+,则KNO3的还原产物为( )
| A、NO2 |
| B、NO |
| C、N2O |
| D、N2O5 |
实验室制取氧气的反应为2KMnO4
K2MnO4+MnO2+3O2↑,反应后从剩余物中回收二氧化锰的操作顺序正确的是( )
| ||
| A、溶解、过滤、洗涤、干燥 |
| B、溶解、过滤、蒸发、洗涤 |
| C、溶解、蒸发、洗涤、过滤 |
| D、溶解、洗涤、过滤、加热 |
下列各组括号内的试剂,能用于除掉物质中杂质的是( )
| A、Fe粉中混有Zn粉杂质(稀H2SO4) |
| B、FeCl2中混有FeCl3杂质(Cl2) |
| C、CO气体中混有CO2杂质(NaOH溶液) |
| D、FeCl3中混有FeCl2杂质(铁屑) |
改变外界条件可以影响化学反应速率,对反应H2(g)+I2(g)?2HI(g),其中能使活化分子百分数增加的是:①升高体系的温度 ②增加反应物浓度 ③增大气体的压强 ④使用催化剂( )
| A、①③ | B、①④ | C、②③ | D、③④ |
氧化还原反应与四种基本类型反应的关系如图所示,则下列属于3区域的是( )

| A、Fe+CuSO4=FeSO4+Cu | ||||
B、2KMnO4
| ||||
| C、4Fe(OH)2+O2+2H2O=4Fe(OH)3 | ||||
| D、2Na2O2+2CO2=2Na2CO3+O2 |
下列有关化学反应速率的说法正确的是( )
| A、用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率 |
| B、100mL2mol/L的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速度减小 |
| C、SO2的催化氧化是一个放热的反应,所以升高温度,V逆加快,V正减慢 |
| D、对于CaCO3+2HCl═CaCl2+H2O+CO2↑不能用CaCO3的浓度变化来表示反应速率,但可用水的浓度变化来表示 |
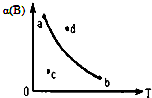 条件一定时,反应2A(g)+B(g)?2C(g),B的转化率α与温度T变化关系曲线图如图所示,图中4个点中,表示未达到平衡状态,且V正<V逆的点是( )
条件一定时,反应2A(g)+B(g)?2C(g),B的转化率α与温度T变化关系曲线图如图所示,图中4个点中,表示未达到平衡状态,且V正<V逆的点是( )