下列关于电解池的叙述中,不正确的是( )
| A、在电解池的阳极发生氧化反应 |
| B、与电源负极相接的是电解池的阴极 |
| C、电子从电源的负极沿导线流向电解池的阴极 |
| D、与电源正极相接的是电解池的阴极 |
已知盐酸和镁反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液:①蒸馏水②NaCl溶液③NaNO3固体④Na2CO3固体⑤CH3COONa固体,你认为可行的是( )
| A、①②③ | B、①②⑤ | C、④ | D、全部 |
 容积均为500 mL的Ⅰ,Ⅱ,Ⅲ三个密闭容器(容器体积恒定不变)中分别充入1 mol N2和2.5 mol H2,三个容器的反应温度分别为T1,T2,T3且恒定不变,在其他条件相同的情况下发生反应:N2+3H2?2NH3(△H<0).实验测得反应均进行到t min时N2的体积分数如图所示.下列说法正确的是( )
容积均为500 mL的Ⅰ,Ⅱ,Ⅲ三个密闭容器(容器体积恒定不变)中分别充入1 mol N2和2.5 mol H2,三个容器的反应温度分别为T1,T2,T3且恒定不变,在其他条件相同的情况下发生反应:N2+3H2?2NH3(△H<0).实验测得反应均进行到t min时N2的体积分数如图所示.下列说法正确的是( )| A、当v(H2)=3v(N2)时,可以说明三个容器中的反应达平衡状态 |
| B、在t min时,一定达化学平衡状态的是Ⅱ和Ⅲ |
| C、在t min时测得c(N2)Ⅲ=1 mol/L,若再向Ⅲ中充入1.5 mol N2和1 mol NH3,H2的转化率不变 |
| D、三个容器中的反应均达到平衡后,容器I中混合气体的平均相对分子质量最小 |
下列相关实验示意图不能达到实验目的是( )
A、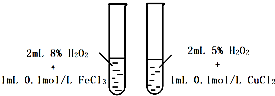 探究不同催化剂对H2O2分解速率影响 |
B、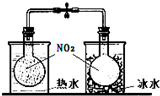 探究温度对2NO2?N2O4平衡影响 |
C、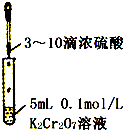 验证Cr2O72-+H2O?2CrO42-+2H+平衡状态变化 |
D、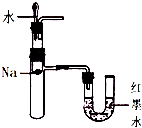 验证钠和水反应的热效应 |
工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对生态系统造成很大的损害,其中还原沉淀法是常用的一种处理方法.流程如下:CrO
Cr2O
Cr3+
Cr(OH)3↓,其中第①步中存在平衡:2CrO42-(黄色)+2H+?Cr2O72-(橙色)+H2O.下列有关说法正确的是( )
2- 4 |
| H+ |
| ①转化 |
2- 7 |
| fe2+ |
| ②还原 |
| 沉淀剂a |
| ③沉淀 |
| A、第①步当2c (Cr2O72-)=c(CrO42-)时,达到了平衡状态 |
| B、对于上述平衡,加入适量稀硫酸后,溶液颜色变黄色,则有利于CrO42-的生成 |
| C、Cr(OH)3是一种两性氢氧化物,所以像Al(OH)3一样能溶于氨水和碳酸溶液中 |
| D、第②步中,还原0.1 mol Cr2O72-需要91.2 g FeSO4 |

 I.某学生设计了如图1所示的装置(框内部分未画出),在装置内起初发生的反应为Cu+H2SO4=H2↑+CuSO4,试回答:
I.某学生设计了如图1所示的装置(框内部分未画出),在装置内起初发生的反应为Cu+H2SO4=H2↑+CuSO4,试回答: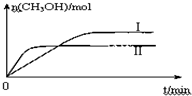 某实验将CO2和H2充入一定体积的密闭容器中,在两种不同条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1
某实验将CO2和H2充入一定体积的密闭容器中,在两种不同条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.