��Ŀ����
ijһ��Ӧ��ϵ�д�������6�����ʣ�NO��FeSO4��Fe��NO3��3��HNO3��Fe2��SO4��3����H2O����֪��������ת����ϵ��HNO3��NO����������и��⣺
��1���÷�Ӧ�Ļ�ԭ���� ��
��2����Ӧ��1mol������ ����õ�����ʧȥ���� mol���ӣ�
��3������0.1mol HNO3����ԭ����ʱ���ɱ�״����NO������� L��
��4����ɷ�Ӧ�ķ���ʽ��
+ = + + + ��
��1���÷�Ӧ�Ļ�ԭ����
��2����Ӧ��1mol������
��3������0.1mol HNO3����ԭ����ʱ���ɱ�״����NO�������
��4����ɷ�Ӧ�ķ���ʽ��
���㣺������ԭ��Ӧ�ļ���
ר�⣺
��������������������У�HNO3�е�Ԫ�ػ��ϼ�λ����ۣ����������ԣ���Ӧ��ԭ����ΪNO���ܽ���ԭ�Ե�FeSO4����ΪFe2��SO4��3��������ԭ���غ㣬ˮ���������У����ݻ��ϼ�������Ⱥ�ԭ���غ���ƽ�����ķ�Ӧ���Դ˽����⣮
���
�⣺��1��������ԭ��Ӧ������Ϊ���ϼ۵���������Ӧ��HNO3Ϊ��Ӧ�����ǿ�����ԣ���NOΪ�������Ӧ�����ᱻ��ԭ��Ϊ�����������������Ԫ�ػ��ϼ۷����仯�Ļ���Fe����FeԪ�ػ��ϼ�Ӧ���ߣ�����������FeSO4ӦΪ��ԭ��������������Fe��NO3��3��Fe2��SO4��3���ʴ�Ϊ��FeSO4��
��2������Ϊ���������ڷ�Ӧ�еõ����ӣ��ɻ��ϼ۱仯��֪NԪ�ػ��ϼ���+5�۽��͵�+2�ۣ���1mol���ᷴӦ�õ�3mol���ӣ��ʴ�Ϊ���õ���3��
��3������0.1mol HNO3����ԭ����ʱ����NO��0.1mol���ڱ�״����NO�������2.24L���ʴ�Ϊ��2.24��
��4�����ݵ����غ㣬��Ԫ�صĻ��ϼ۽�����3�ۣ���Ԫ�ػ��ϼ�������1�ۣ����ݵ�ʧ�����غ��Լ�Ԫ���غ㣬������������ǰ��ϵ����3������ǰϵ����4��ˮ��ǰ��ϵ����2������ʽΪ��4HNO3+3FeSO4=Fe��NO3��3+Fe2��SO4��3+NO��+2H2O
�ʴ�Ϊ��4HNO3��3FeSO4��Fe2��SO4��3��Fe��NO3��3��NO����2H2O��
��2������Ϊ���������ڷ�Ӧ�еõ����ӣ��ɻ��ϼ۱仯��֪NԪ�ػ��ϼ���+5�۽��͵�+2�ۣ���1mol���ᷴӦ�õ�3mol���ӣ��ʴ�Ϊ���õ���3��
��3������0.1mol HNO3����ԭ����ʱ����NO��0.1mol���ڱ�״����NO�������2.24L���ʴ�Ϊ��2.24��
��4�����ݵ����غ㣬��Ԫ�صĻ��ϼ۽�����3�ۣ���Ԫ�ػ��ϼ�������1�ۣ����ݵ�ʧ�����غ��Լ�Ԫ���غ㣬������������ǰ��ϵ����3������ǰϵ����4��ˮ��ǰ��ϵ����2������ʽΪ��4HNO3+3FeSO4=Fe��NO3��3+Fe2��SO4��3+NO��+2H2O
�ʴ�Ϊ��4HNO3��3FeSO4��Fe2��SO4��3��Fe��NO3��3��NO����2H2O��
���������⿼��������ԭ��Ӧ��ѧ����ʽ����д�������ڴӻ��ϼ۷�����������ͻ�ԭ�����ԭ���غ�ȷ��������Ӧ��������ݸ��ݵ����غ�������غ�����ƽ����ʽ����Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
�����Ŀ
���й������ϵ�����������ǣ�������
| A�������Ǿۺ��� |
| B��CH2=CH-CH3�Ǿ���ϩ�ĵ��� |
| C�����ϵ���Ҫ�ɷ��Ǻϳ���֬ |
| D�����Ͽ��Է�Ϊ�ȹ��Ժ������� |
 �ݻ���Ϊ500 mL�Ģ������ܱ���������������㶨���䣩�зֱ����1 mol N2��2.5 mol H2�����������ķ�Ӧ�¶ȷֱ�ΪT1��T2��T3�Һ㶨���䣬������������ͬ������·�����Ӧ��N2+3H2?2NH3����H��0����ʵ���÷�Ӧ�����е�t minʱN2�����������ͼ��ʾ������˵����ȷ���ǣ�������
�ݻ���Ϊ500 mL�Ģ������ܱ���������������㶨���䣩�зֱ����1 mol N2��2.5 mol H2�����������ķ�Ӧ�¶ȷֱ�ΪT1��T2��T3�Һ㶨���䣬������������ͬ������·�����Ӧ��N2+3H2?2NH3����H��0����ʵ���÷�Ӧ�����е�t minʱN2�����������ͼ��ʾ������˵����ȷ���ǣ�������| A����v��H2��=3v��N2��ʱ������˵�����������еķ�Ӧ��ƽ��״̬ |
| B����t minʱ��һ���ﻯѧƽ��״̬���Ǣ�͢� |
| C����t minʱ���c��N2����=1 mol/L����������г���1.5 mol N2��1 mol NH3��H2��ת���ʲ��� |
| D�����������еķ�Ӧ���ﵽƽ�������I�л�������ƽ����Է���������С |
��֪�Ȼ�ѧ����ʽ����������ȼ����Ϊ��������
��H2��g��+
O2��g���TH2O��g����H=-241.8kJ?mol-1
��2H2��g��+O2��g���T2H2O��g����H=-483.6kJ?mol-1
��H2��g��+
O2��g���TH2O��l����H=-285.8kJ?mol-1
��2H2��g��+O2��g���T2H2O��l����H=-571.6kJ?mol-1?
��H2��g��+
| 1 |
| 2 |
��2H2��g��+O2��g���T2H2O��g����H=-483.6kJ?mol-1
��H2��g��+
| 1 |
| 2 |
��2H2��g��+O2��g���T2H2O��l����H=-571.6kJ?mol-1?
| A��-241.8 kJ?mol-1 |
| B��-483.6 kJ?mol-1 |
| C��-285.8 kJ?mol-1 |
| D��-571.6 kJ?mol-1 |
��ͼ��ƿ�����ȵ����壬��ͬ��ͬѹʱƿ������Ĺ�ϵһ����ȷ���ǣ�������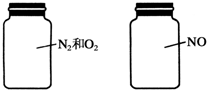

| A��������������� |
| B�������ܶ���� |
| C������ԭ������� |
| D��Ħ��������� |
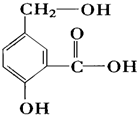 ��1���ù�ҵ�ƾ�����ļپ���ͨ������
��1���ù�ҵ�ƾ�����ļپ���ͨ������