0 131001 131009 131015 131019 131025 131027 131031 131037 131039 131045 131051 131055 131057 131061 131067 131069 131075 131079 131081 131085 131087 131091 131093 131095 131096 131097 131099 131100 131101 131103 131105 131109 131111 131115 131117 131121 131127 131129 131135 131139 131141 131145 131151 131157 131159 131165 131169 131171 131177 131181 131187 131195 203614

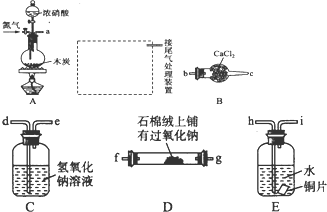




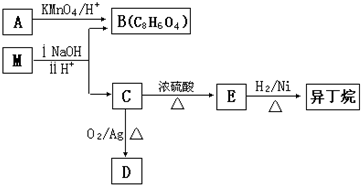 苯的同系物是人类最早认识的芳香族化合物,其中对二甲苯(英文名称p-xylene,缩写为PX)是化学工业的重要原料.
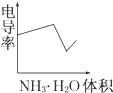
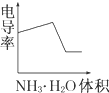
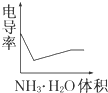
苯的同系物是人类最早认识的芳香族化合物,其中对二甲苯(英文名称p-xylene,缩写为PX)是化学工业的重要原料. 电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率变化可以确定滴定反应的终点.如图是用KOH溶液分别滴定HCl溶液和CH3COOH溶液的滴定曲线示意图.
电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率变化可以确定滴定反应的终点.如图是用KOH溶液分别滴定HCl溶液和CH3COOH溶液的滴定曲线示意图.