将m g铁粉放入含有x mol FeCl3和y molCuCl2的混合溶液中,充分反应后,固体质量仍为m g.则x:y可能是( )
| A、2:7 | B、1:7 |
| C、8:7 | D、1:1 |
已知M、W、X、Y、Z是短周期中原子序数依次增大的5种主族元素,其中W、Z同族,M原子的最外层电子数是电子层数的3倍,元素X在同周期的主族元素中原子半径最大,Y是地壳中含量最多的金属元素.下列说法中正确的是( )
| A、气态氢化物稳定性最强的是HZ |
| B、原子半径由小到大的顺序为W<M<Y |
| C、室温下,可用Y的容器盛装稀硝酸 |
| D、X的单质可通过电解XZ的水溶液获得 |
用足量的MnO2和含HCl为4mol的浓盐酸充分反应(共热),在不考虑HCl挥发的情况下,得到的氯气( )
| A、等于2mol |
| B、等于1mol |
| C、小于1mol |
| D、大于2mol |
下列现象或新技术的应用中,不涉及胶体性质的是( )
| A、在饱和氯化铁溶液中滴加NaOH溶液,产生红褐色沉淀 |
| B、使用微波手术刀进行外科手术,可使开刀处的血液迅速凝固而减少失血 |
| C、清晨,在茂密的树林中,常常可以看到枝叶间透过的一道道光线 |
| D、肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗 |
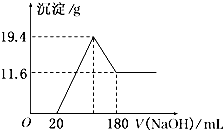 将可能含有少量碳、硅杂质的a克镁铝合金投入100mL一定物质的量浓度的盐酸中,合金部分溶解,过滤,向所得溶液中滴加5mol/L NaOH溶液至过量,生成沉淀的质量与加入氢氧化钠溶液的体积的关系如图所示.
将可能含有少量碳、硅杂质的a克镁铝合金投入100mL一定物质的量浓度的盐酸中,合金部分溶解,过滤,向所得溶液中滴加5mol/L NaOH溶液至过量,生成沉淀的质量与加入氢氧化钠溶液的体积的关系如图所示.