题目内容
用足量的MnO2和含HCl为4mol的浓盐酸充分反应(共热),在不考虑HCl挥发的情况下,得到的氯气( )
| A、等于2mol |
| B、等于1mol |
| C、小于1mol |
| D、大于2mol |
考点:化学方程式的有关计算
专题:
分析:MnO2与浓HCl反应,随着反应的进行,浓HCl变稀,稀盐酸不能与MnO2反应,以此解答.
解答:
解:实验室制取氯气的化学方程式为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,假设含HCl为4mol的浓盐酸能完全反应,则生成氯气为1mol,而MnO2不能氧化稀盐酸,随着反应的进行,浓HCl变稀,稀盐酸不能与MnO2反应,故反应中产生的氯气小于1mol,
故选C.
| ||
故选C.
点评:本题考查氯气的制备,题目难度不大,注意氯气的实验室制法以及浓稀盐酸的性质的差异性,注意稀盐酸与二氧化锰不反应.

练习册系列答案
相关题目
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
A、已知:
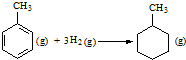 的△H为-384 kJ?mol-1 的△H为-384 kJ?mol-1 | ||||||||||
| B、将足量SO2通入Ba(NO3)2溶液中有沉淀生成的离子方程式,3SO2+Ba2++2NO3-+2H2O=BaSO4↓+2NO+2SO42-+4H+ | ||||||||||
| C、电解稀硫酸不可能发生的反应:Cu+H2SO4=CuSO4+H2↑ | ||||||||||
| D、1000℃时,Na2SO4与H2发生反应:Na2SO4(s)+4H2(g)?Na2S(s)+4H2O(g)△H>0,反应达到平衡后,将体系中的Na2S(s)全部移走,平衡不移动 |
从下列事实,找出不能用勒沙特列原理解释的是( )
| A、在溴水中存在如下平衡:Br2+H2O=HBr+HBrO,当加入NaOH溶液后颜色变浅 |
| B、对2HI?H2+I2(气)平衡体系增加压强使颜色变深 |
| C、反应CO+NO2?CO2+NO(△H<0)升高温度使平衡向逆方向移动 |
| D、合成氨反应:N2+3H2?2NH3(△H<0),为使氨的产率提高,理论上应采取低温高压的措施 |
与100mL 0.1mol/LNa2SO4溶液中Na+离子浓度相同的是( )
| A、10mL 1mol/L Na2SO4溶液 |
| B、50mL 0.2mol/L NaCl溶液 |
| C、10mL 0.2mol/LNa2SO4溶液 |
| D、200mL 0.1mol/L NaNO3溶液 |
X、Y、Z为同一短周期中的元素,其原子半径依次减小,它们的最高价氧化物对应的水化物之间,任意两种混合均可反应,M为Y、Z形成的化合物,其溶液显酸性.下列说法正确的是( )
| A、X、Y、Z简单离子的半径依次增大 |
| B、将M溶液加热蒸干并灼烧,最后可得Y的氧化物 |
| C、Y的最高价氧化物为碱性氧化物 |
| D、将少量X单质投入到M溶液中,会置换出Y单质 |
工业上制备HNO3的最后一步方程式为:3NO2+H2O═2HNO3+NO,发生还原反应和氧化反应的物质的质量比为( )
| A、3:1 | B、1:3 |
| C、1:2 | D、2:1 |