下列离子方程式正确的是( )
| A、向AlCl3溶液滴入过量氨水:Al3++4OH-=AlO2-+2H2O | ||
B、用银氨溶液检验乙醛中的醛基:CH3CHO+2Ag(NH3)2++2OH-
| ||
| C、苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O-→2C6H5OH+2CO32- | ||
| D、Na2SO3溶液使酸性KMnO4溶液褪色:5SO32-+4H++2MnO4-=5SO42-+2Mn2++2H2O |
下列离子方程式正确的是( )
| A、稀硝酸与氢氧化钾溶液反应 H++OH-=H2O |
| B、铝与稀盐酸反应 Al+2H+=Al3++H2↑ |
| C、三氯化铁溶液与氢氧化钠溶液反应 FeCl3+3OH-=Fe(OH)3↓+3Cl- |
| D、足量二氧化碳与澄清石灰水反应 CO2+2OH-=CO32-+H2O |
下列有关实验操作、现象或实验原理的叙述,错误的是( )
| A、减压过滤不宜用于过滤胶状沉淀或颗粒太小的沉淀,沉淀的颗粒较大时,可用倾析法将固体与溶液分离 |
| B、制备阿司匹林时,将反应物置于水浴85~90℃的锥形瓶中充分反应5~10min,冷却后,向锥形瓶中加一定量的水可以促进产物的析出 |
| C、牙膏中的安息香酸钠、氟化钠溶于水,水解使溶液呈碱性,可以预防龋齿 |
| D、由Zn-Cu/稀硫酸构成的原电池溶液中加入适量的H2O2能提高电池的放电效率 |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、常温常压下,8gO2的体积为5.6L |
| B、标准状况下,22.4LCCl4所含的分子数为NA |
| C、标准状况下,1.8gH2 O中含有电子数为NA |
| D、常温常压下,10g氖气含有的原子数为NA |
下列说法中正确的是(NA表示阿伏伽德罗常数)( )
| A、28g N2所含有的原子数为NA |
| B、1.8g的NH4+离子中含有电子数11NA |
| C、22.4LCH4的质量与NA个甲烷分子的质量之和相等 |
| D、标准状况下,22.4LCH4和O2的混合气体所含有的分子数为NA |
NA为阿伏伽德罗常数,下列叙述错误的是( )
| A、标准状况下,11.2 L氦气中含有0.5 NA原子 |
| B、常温常压下,46g NO2和N2O4混合气体中含有原子总数为3NA |
| C、标准状况下,0.1 mol Cl2参加反应,转移的电子数目一定为0.2 NA |
| D、1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,转移电子总数NA个 |
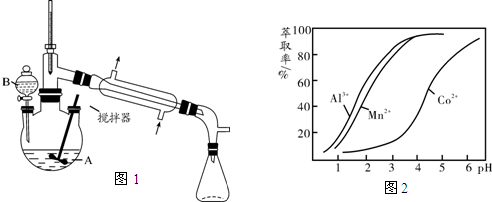
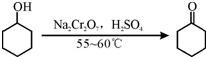 其反应的装置示意图如图1(夹持装置、加热装置略去):
其反应的装置示意图如图1(夹持装置、加热装置略去):