题目内容
下列说法中正确的是(NA表示阿伏伽德罗常数)( )
| A、28g N2所含有的原子数为NA |
| B、1.8g的NH4+离子中含有电子数11NA |
| C、22.4LCH4的质量与NA个甲烷分子的质量之和相等 |
| D、标准状况下,22.4LCH4和O2的混合气体所含有的分子数为NA |
考点:阿伏加德罗常数
专题:
分析:A.依据n=
计算物质的量结合氮气是双原子分子计算原子数;
B.1个NH4+离子含有10个电子;
C.没指明气体的状况,Vm不确定;
D.标况下1mol任何气体的体积约为22.4L.
| m |
| M |
B.1个NH4+离子含有10个电子;
C.没指明气体的状况,Vm不确定;
D.标况下1mol任何气体的体积约为22.4L.
解答:
解:A.28g氮气物质的量=
=1mol,含有的原子数为2NA,故A错误;
B.1个NH4+离子含有10个电子,1.8g的NH4+离子的物质的量=
=0.1mol,含有电子数1NA,故B错误;
C.没指明气体的状况,Vm不一定等于22.4L/mol,无法判断,故C错误;
D.标准状况下,22.4LCH4和O2的混合气体物质的量为1mol,含有分子数为NA,故D正确;
故选:D.
| 28g |
| 28g/mol |
B.1个NH4+离子含有10个电子,1.8g的NH4+离子的物质的量=
| 1.8g |
| 18g/mol |
C.没指明气体的状况,Vm不一定等于22.4L/mol,无法判断,故C错误;
D.标准状况下,22.4LCH4和O2的混合气体物质的量为1mol,含有分子数为NA,故D正确;
故选:D.
点评:本题考查了阿伏伽德罗常数的计算及判断,掌握阿伏伽德罗常数与物质的量、摩尔质量等物理量之间的转化,明确标况下气体摩尔体积的使用条件是解题关键,题目难度不大.

练习册系列答案
 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目
下列说法正确的是( )
| A、难溶电解质作比较时,Ksp小的,溶解度一定小 |
| B、Ksp大小取决于难溶电解质的量,所以离子浓度改变时,沉淀平衡会发生移动 |
| C、所谓沉淀完全就是用沉淀剂将溶液中某一离子完全除去 |
| D、温度一定,当溶液中Ag+ 和Cl-浓度的乘积等于Ksp时,溶液为AgCl的饱和溶液 |
下列溶液中各微粒的浓度关系一定正确的是( )
| A、25°C时,pH=10的CH3COONa溶液与pH=10的氨水中,c(OH-)之此为1:1 |
| B、在Na2CO3和NaHCO3的混合溶液中:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-) |
| C、浓度相同的①CH3COONa②NaNO3③Na2CO3④NaOH四种溶液,pH的大小顺序是:④>③>②>① |
| D、只含NH4+、Cl-、H+、OH-四种离子的酸性溶液中,一定存在:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
有关如图及实验的描述不正确的是( )
A、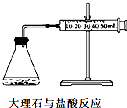 可以测量大理石与盐酸的反应速率 |
B、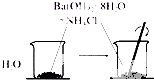 说明吸热反应也可能是自发反应 |
C、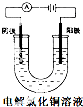 两个电极都为铜片时,电解初期溶液的浓度基本不改变 |
D、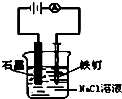 实验中,铁钉上会有刺激性气体产生 |
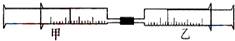 如图所示,在25℃、101.3KPa下将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质缓慢压到甲针筒内,进行下表所列的不同实验.下列说法不正确的是( )
如图所示,在25℃、101.3KPa下将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质缓慢压到甲针筒内,进行下表所列的不同实验.下列说法不正确的是( )| 实验序号 | 甲针筒 | 乙针筒 |
| 1 | 10mLH2S | 10mLSO2 |
| 2 | 30mLNO2 | 10mLH2O |
| 3 | 20mLNO | 10mLO2 |
| 4 | 10mLCCl4 | 10mLHCl |
| A、实验1,甲中活塞不移动,有黄色固体生成 |
| B、实验2,甲中活塞向右移动,剩余的无色气体是NO |
| C、实验3,甲中活塞不移动,充满红棕色气体 |
| D、实验4,甲中活塞向左移动 |
下列离子方程式正确的是( )
| A、向AlCl3溶液滴入过量氨水:Al3++4OH-=AlO2-+2H2O | ||
B、用银氨溶液检验乙醛中的醛基:CH3CHO+2Ag(NH3)2++2OH-
| ||
| C、苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O-→2C6H5OH+2CO32- | ||
| D、Na2SO3溶液使酸性KMnO4溶液褪色:5SO32-+4H++2MnO4-=5SO42-+2Mn2++2H2O |
有关下列高分子材料叙述正确的是( )
| A、塑料是以石油、天然气为原料,以二烯烃和烯烃为单体聚合成的高分子 |
| B、光导纤维是一种能高质量传导光的玻璃纤维,属于具有特殊性能的合成纤维 |
| C、塑料制品在土壤中容易被微生物分解,所以废弃塑料制品不会对环境造成严重的污染 |
| D、工程塑料具有某些优异的性能,可作为工程材料代替某些金属 |
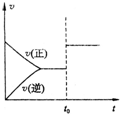 某温度下,将2mol A和3mol B充入一密闭容器中,发生反应aA(g)+B(g)?C(g)+D(g),5min后达到平衡.已知该温度下其平衡常数K=1,在t0时刻,若保持温度不变将容器体积扩大为原来的10倍,A的转化率不发生变化,则下列说法正确的是( )
某温度下,将2mol A和3mol B充入一密闭容器中,发生反应aA(g)+B(g)?C(g)+D(g),5min后达到平衡.已知该温度下其平衡常数K=1,在t0时刻,若保持温度不变将容器体积扩大为原来的10倍,A的转化率不发生变化,则下列说法正确的是( )| A、a=2 |
| B、达平衡时A的转化率为60% |
| C、速率随时间变化关系如右图所示 |
| D、为提高A的转化率,可采取升高温度的措施 |