题目内容
写出下列反应的离子方程式
(1)用稀硫酸清除铁锈(Fe2O3):
(2)硫酸铜溶液和氢氧化钡溶液:
(3)FeCl3溶液中加入NaOH溶液: .
(1)用稀硫酸清除铁锈(Fe2O3):
(2)硫酸铜溶液和氢氧化钡溶液:
(3)FeCl3溶液中加入NaOH溶液:
考点:离子方程式的书写
专题:
分析:(1)反应生成硫酸铁和水,氧化铁、水在离子反应中保留化学式;
(2)反应生成硫酸钡和氢氧化铜;
(3)反应生成氢氧化铁和氯化钠,结合离子反应的书写方法来解答.
(2)反应生成硫酸钡和氢氧化铜;
(3)反应生成氢氧化铁和氯化钠,结合离子反应的书写方法来解答.
解答:
解:(1)反应生成硫酸铁和水,离子反应为Fe2O3+6H+=3H2O+2Fe3+,故答案为:Fe2O3+6H+=3H2O+2Fe3+;
(2)反应生成硫酸钡和氢氧化铜,离子反应Ba2++SO42-+Cu2++2OH-=Cu(OH)2↓+BaSO4↓,故答案为:Ba2++SO42-+Cu2++2OH-=Cu(OH)2↓+BaSO4↓;
(3)反应生成氢氧化铁和氯化钠,离子反应为Fe3++3OH-=Fe(OH)3↓,故答案为:Fe3++3OH-=Fe(OH)3↓.
(2)反应生成硫酸钡和氢氧化铜,离子反应Ba2++SO42-+Cu2++2OH-=Cu(OH)2↓+BaSO4↓,故答案为:Ba2++SO42-+Cu2++2OH-=Cu(OH)2↓+BaSO4↓;
(3)反应生成氢氧化铁和氯化钠,离子反应为Fe3++3OH-=Fe(OH)3↓,故答案为:Fe3++3OH-=Fe(OH)3↓.
点评:本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应的离子反应考查,注意离子反应中保留化学式的物质,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列与有机物的结构、性质相关的叙述错误的是( )
| A、分子式为C5H12的烃有三种可能的结构 |
| B、乙醇分子中含有羟基,可以和金属Na反应生成H2 |
| C、苯不能使溴的四氯化碳溶液褪色,说明苯分子中没有与乙烯分子中相似的碳碳双键 |
| D、淀粉、蛋白质、油脂、葡萄糖在一定条件下均能发生水解反应 |
下列基本操作正确的是( )
| A、配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸 |
| B、用燃着的酒精灯去点燃另一盏酒精灯 |
| C、用天平称取药品时用手直接拿砝码 |
| D、用滴管滴加液体时,滴管应垂悬在容器上方,不能触及容器内壁 |
NA为阿伏伽德罗常数,下列叙述错误的是( )
| A、标准状况下,11.2 L氦气中含有0.5 NA原子 |
| B、常温常压下,46g NO2和N2O4混合气体中含有原子总数为3NA |
| C、标准状况下,0.1 mol Cl2参加反应,转移的电子数目一定为0.2 NA |
| D、1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,转移电子总数NA个 |
设阿伏加德罗常数为NA.则下列说法正确的是( )
| A、0.1 mo1?L-1稀硫酸100mL中含有硫酸根的个数为0.1NA | ||
B、1 cm3铁所含的铁原子数是
| ||
| C、常温下,2.7g 铝片投入足量的浓硫酸中,铝失去的电子数为0.3NA | ||
| D、2.24L CO2与足量的Na2O2转移的电子总数可能为0.1NA |
生产生活离不开化学,下列有关说法,你的判断是( )
①“白雪牌”漂粉精可令所有有色物质黯然失“色”,没有最白,只有更白
②“农夫山泉”天然矿泉水不含任何化学物质
③人喝了啤酒会打嗝,是因为啤酒中的碳酸盐与胃酸反应生成了二氧化碳
④53度白酒是指乙醇的质量分数为53%
⑤“碳纳米泡沫”是一种纯碳新材料,每个泡沫直径约6到9nm,该材料能产生丁达尔现象
⑥“静心”口服液含丰富的氮、磷、锌等微量元素.
①“白雪牌”漂粉精可令所有有色物质黯然失“色”,没有最白,只有更白
②“农夫山泉”天然矿泉水不含任何化学物质
③人喝了啤酒会打嗝,是因为啤酒中的碳酸盐与胃酸反应生成了二氧化碳
④53度白酒是指乙醇的质量分数为53%
⑤“碳纳米泡沫”是一种纯碳新材料,每个泡沫直径约6到9nm,该材料能产生丁达尔现象
⑥“静心”口服液含丰富的氮、磷、锌等微量元素.
| A、全都正确 |
| B、只有⑤正确 |
| C、只有④⑤正确 |
| D、以上说法都是错误的 |
常温下,若等物质的量浓度的HA溶液和NaOH溶液混合后pH=7,下列说法合理的是( )
| A、反应后HA溶液一定没有剩余 |
| B、生成物NaA的水溶液的pH可能小于7 |
| C、HA溶液和NaOH溶液的体积可能不相等 |
| D、HA溶液的c(H+)和NaOH溶液的c(OH-)一定相等 |
化学在生产和日常生活中有着重要的应用.下列叙述正确的是( )
| A、盐酸滴定氨水,可以选择酚酞为指示剂 |
| B、电离程度(同温度同浓度溶液中):HCl>CH3OOH>NaHCO3 |
| C、分散质粒子的直径:FeCl3溶液>Fe(OH)3胶体>Fe(OH)3悬浊液 |
| D、若要使Na2S溶液中c(Na+)/c(S2-)的值减小,可以加入适量的KOH固体 |
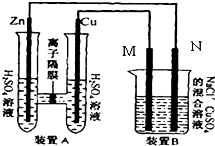 如图装置B中是浓度均为0.1mol/L的NaCl、CuSO4混合溶液,溶液体积为500ml,M、N均为石墨电极,当装置A中Zn棒质量减少6.5g时,N上质量增加
如图装置B中是浓度均为0.1mol/L的NaCl、CuSO4混合溶液,溶液体积为500ml,M、N均为石墨电极,当装置A中Zn棒质量减少6.5g时,N上质量增加