常温下,下列溶液中有关物质的量浓度关系和计算不正确的是( )
| A、c(NH4+)相等的(NH4)2SO4、(NH4)2Fe(SO4)2和NH4C1溶液中,溶质物质的量浓度大小关系是:c(NH4Cl)>c[(NH4)2SO4]>c[(NH4)2Fe(SO4)2] |
| B、已知25℃时Ksp(AgCl)=1.8×10-10,则在0.1 mol?L-l A1Cl3溶液中,Ag+的物质的量浓度最大可达到6.0×10-10mol?L-l |
| C、25℃时0.2 mol?L-l HC1溶液与等体积0.05 mol?L-l Ba(OH)2溶液混合后,溶液的pH约为1 |
| D、0.1mol?L-l NaHA溶液的pH=4,则有c(HA-)>c(H+)>c(A2-)>c(H2A) |
下列化学药品的贮存方法正确的是( )
| A、浓硝酸存放在带玻璃塞的无色细口瓶中 |
| B、少量碘储存在酒精中 |
| C、氢氧化钠固体保存在带橡胶塞的广口瓶中 |
| D、少量金属钠保存在煤油、四氯化碳等有机溶剂中 |
在如图装置中,若通电一段时间后乙装置左侧电极质量增加,下列说法错误的是( )


| A、当甲装置中共产生标准状况下4.48 L气体时,Cu电极上质量增加43.2g |
| B、电解过程中装置丙的pH无变化 |
| C、丙中硝酸银溶液的浓度不变 |
| D、乙中左侧电极反应式:Cu2++2e-=Cu |
下列物质的贮存方法,错误的是( )
| A、钠存入在煤油里 |
| B、硝酸存放在无色试剂瓶中 |
| C、生产上用铝槽车装浓硝酸 |
| D、烧碱溶液存放在橡皮塞的试剂瓶中 |
如图所示装置中,a、b都是惰性电极,通电一段时间后,a极附近溶液呈红色.下列说法正确的是( )
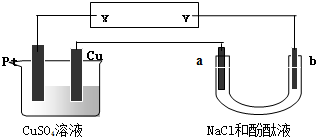

| A、NaCl溶液浓度不变 |
| B、X是负极,Y是正极 |
| C、CuSO4溶液浓度变小 |
| D、X是正极,Y是负极 |
下列试剂的贮存方法不正确的是( )
| A、氢氧化钠固体应密封贮存于塑料瓶中 |
| B、碘固体保存在棕色细口瓶中 |
| C、氯水贮存在棕色细口瓶中 |
| D、溴存放在试剂瓶里,并往瓶中加一些水进行液封 |
下列各组离子在无色水溶液中能大量共存的是( )
| A、Na+Mg2+Cl-OH- |
| B、MnO4- HCO3- OH- K+ |
| C、Fe3+ H+ SO42- CH3COO- |
| D、K+ NO3- CO32- Na+ |
使用容量瓶配置溶液时,由于操作不当会引起误差,下列情况会使所配溶液浓度偏低的是( )
①溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
②转移溶液前容量瓶内有少量蒸馏水
③定容时,仰视容量瓶的刻度线
④定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线.
①溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
②转移溶液前容量瓶内有少量蒸馏水
③定容时,仰视容量瓶的刻度线
④定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线.
| A、②③④ | B、①②③ |
| C、①③④ | D、①②③④ |
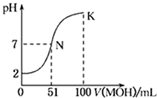 常温下,向l00mL 0.01mol/L HA的溶液中逐滴加入0.02mol/L MOH溶液,如图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中正确的是( )
常温下,向l00mL 0.01mol/L HA的溶液中逐滴加入0.02mol/L MOH溶液,如图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中正确的是( )| A、HA为一元强酸,MOH为一元强碱 |
| B、N点水的电离程度小于K点水的电离程度 |
| C、K点所示溶液中c(A-)>c(M+) |
| D、K点对应的溶液中,有c(MOH)+c(M+)=0.01mol/L |
某位同学配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )
| A、所用NaOH已经潮解 |
| B、定容时仰视刻度线 |
| C、有少量NaOH溶液残留在烧杯里 |
| D、称量时所用砝码生锈 |