题目内容
常温下,下列溶液中有关物质的量浓度关系和计算不正确的是( )
| A、c(NH4+)相等的(NH4)2SO4、(NH4)2Fe(SO4)2和NH4C1溶液中,溶质物质的量浓度大小关系是:c(NH4Cl)>c[(NH4)2SO4]>c[(NH4)2Fe(SO4)2] |
| B、已知25℃时Ksp(AgCl)=1.8×10-10,则在0.1 mol?L-l A1Cl3溶液中,Ag+的物质的量浓度最大可达到6.0×10-10mol?L-l |
| C、25℃时0.2 mol?L-l HC1溶液与等体积0.05 mol?L-l Ba(OH)2溶液混合后,溶液的pH约为1 |
| D、0.1mol?L-l NaHA溶液的pH=4,则有c(HA-)>c(H+)>c(A2-)>c(H2A) |
考点:离子浓度大小的比较
专题:
分析:A.根据溶质的化学式、盐的水解原理的影响判断溶质物质的量浓度大小;
B.依据一定温度下沉淀溶解平衡中存在溶度积常数,然后根据溶度积和沉淀溶解平衡,计算银离子最大浓度;
C.先判断溶液酸碱性,然后计算出溶液中氢离子或氢氧根离子浓度,再计算出混合液中氢离子浓度及溶液的pH;
D.0.1mol?L-1的NaHA溶液的pH=4,则HA-的电离程度大于其水解程度,据此判断溶液中各离子浓度大小.
B.依据一定温度下沉淀溶解平衡中存在溶度积常数,然后根据溶度积和沉淀溶解平衡,计算银离子最大浓度;
C.先判断溶液酸碱性,然后计算出溶液中氢离子或氢氧根离子浓度,再计算出混合液中氢离子浓度及溶液的pH;
D.0.1mol?L-1的NaHA溶液的pH=4,则HA-的电离程度大于其水解程度,据此判断溶液中各离子浓度大小.
解答:
解:A.(NH4)2SO4溶液中硫酸根离子对铵根离子水解无影响,(NH4)2Fe(SO4)2和溶液中亚铁离子水解显酸性抑制铵根离子的水解,NH4Cl溶液中氯离子对铵根离子无影响,当铵根离子浓度相同时溶质浓度应为:c(NH4Cl)>c[(NH4)2SO4]>c[(NH4)2Fe(SO4)2],故A正确;
B.Ksp(AgCl)=1.8×10-10,0.1mol?L-1AlCl3溶液中c(Cl-)为0.3mol?L-1,Ksp(AgCl)=c(Ag+)×c(Cl-)=c(Ag+)×0.3mol?L-1=1.8×10-10,解得:c(Ag+)=
=6×10-10mol?L-1,故B正确;
C.0.2mol?L-1 HCl溶液与等体积0.05mol?L-1 Ba(OH)2溶液混合后,依据溶液中溶质物质的量分析判断,酸过量,设酸碱溶液体积为1L,盐酸溶液中氢离子物质的量为:0.2mol/L×1L=0.2mol,氢氧化钡溶液中氢氧根离子物质的量为:0.05mol/L×2×1L=0.1mol,所以混合溶液中c(H+)=
=0.05mol?L-1,溶液的pH=-lg0.05=2-lg5,故C错误;
D.0.1mol?L-1 NaHA溶液的pH=4,溶液呈酸性,说明酸式酸根离子的电离程度大于水解程度,溶液中的离子浓度大小顺序为:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(H2A),故D正确;
故选C.
B.Ksp(AgCl)=1.8×10-10,0.1mol?L-1AlCl3溶液中c(Cl-)为0.3mol?L-1,Ksp(AgCl)=c(Ag+)×c(Cl-)=c(Ag+)×0.3mol?L-1=1.8×10-10,解得:c(Ag+)=
| 1.8×10-10 |
| 0.3mol/L |
C.0.2mol?L-1 HCl溶液与等体积0.05mol?L-1 Ba(OH)2溶液混合后,依据溶液中溶质物质的量分析判断,酸过量,设酸碱溶液体积为1L,盐酸溶液中氢离子物质的量为:0.2mol/L×1L=0.2mol,氢氧化钡溶液中氢氧根离子物质的量为:0.05mol/L×2×1L=0.1mol,所以混合溶液中c(H+)=
| 0.2mol-0.1mol |
| 2L |
D.0.1mol?L-1 NaHA溶液的pH=4,溶液呈酸性,说明酸式酸根离子的电离程度大于水解程度,溶液中的离子浓度大小顺序为:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(H2A),故D正确;
故选C.
点评:本题考查了离子浓度大小比较、难溶物溶解平衡及其计算、酸碱混合的定性判断等知识,题目难度中等,试题知识点较大、综合性较强,充分考查了学生的分析、理解能力及化学计算能力.

练习册系列答案
相关题目
下列各组物质可按照溶解、过滤、蒸发的操作顺序分离的是( )
| A、食盐和泥沙 |
| B、食盐和硝酸钾 |
| C、铁粉和锌粉 |
| D、水和酒精 |
某无色混合气体可能含有CO2、CO、H2O(g)、H2中的一种或几种,依次进行如下处理(假设每次处理均反应完全):①通过碱石灰,气体体积减小;②通过灼热的氧化铜时,固体变为红色;③通过无水CuSO4粉末时,粉末变为蓝色;④通过澄清石灰水时,溶液变为浑浊.由此可以确定混合气体中( )
| A、一定含有CO2、H2O蒸气,可能含有H2、CO |
| B、一定含有H2O蒸气、CO,可能含有CO2、H2 |
| C、一定含有CO2、CO,可能含有H2O蒸气、H2 |
| D、一定含有CO、H2,可能含有H2O蒸气、CO2中的1种或2种 |
下列试剂的贮存方法不正确的是( )
| A、氢氧化钠固体应密封贮存于塑料瓶中 |
| B、碘固体保存在棕色细口瓶中 |
| C、氯水贮存在棕色细口瓶中 |
| D、溴存放在试剂瓶里,并往瓶中加一些水进行液封 |
实验室中配制250mL 0.5mo1?L-1盐酸时,不需要用到的仪器是( )
| A、酒精灯 | B、玻璃棒 |
| C、容量瓶 | D、胶头滴管 |
下列有关物质性质或用途的说法正确的是( )
| A、浓硫酸可用作干燥剂是因为其具有强氧化性 |
| B、利用Al2O3制作的坩埚,可用于熔融烧碱 |
| C、制水泥和玻璃都用石灰石作原料 |
| D、铜的金属活泼性比铁的弱,铜不能与任何强酸发生反应. |
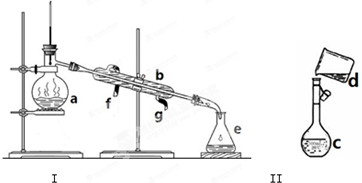 掌握仪器名称、组装及使用方法是中学化学实验的基础,如图为两套实验装置.
掌握仪器名称、组装及使用方法是中学化学实验的基础,如图为两套实验装置.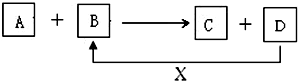 A、B、C、D、X均为中学化学常见的物质.它们之间存在如图所示转化关系(图中反应条件略去)
A、B、C、D、X均为中学化学常见的物质.它们之间存在如图所示转化关系(图中反应条件略去)