某校化学兴趣小组欲用盐酸和锌粒制取氢气,他们在实验室分别取了两瓶盐酸,a瓶标有“HCl,12%”,b瓶标有“HCl,2mol?L-1”,下面是小组成员对两瓶盐酸的叙述正确的是( )
| A、a瓶中含有的溶质HCl比b瓶的多 |
| B、将b瓶加水稀释为原来体积的2倍,盐酸的物质的量浓度不变 |
| C、从b瓶中取出十分之一溶液,溶质HCl的物质的量变为0.2 mol |
| D、a瓶盐酸的物质的量浓度因未知溶液的密度无法计算 |
等物质的量浓度的KCl、MgCl2、AlCl3三种溶液.现欲完全沉淀其中的Cl-,消耗相同物质的量浓度的AgNO3溶液的体积比为3:2:1,则上述三种溶液的体积比为( )
| A、1:1:1 |
| B、6:3:2 |
| C、3:2:1 |
| D、9:3:1 |
配制0.4mol/L的硫酸溶液250mL,需要18mol/L的硫酸溶液的体积是( )
| A、6.0mL |
| B、5.9mL |
| C、5.1mL |
| D、5.6mL |
下列物质中,易溶于水的是( )
| A、KNO3 |
| B、BaSO4 |
| C、AgCl |
| D、CuO |
100mL0.3mol?L-1Na2SO4溶液和50mL0.2mol?L-1Al2(SO4)3溶液混合后,溶液中SO42-离子的物质的量浓度(设体积为二者之和)为( )
| A、0.2mol?L-1 |
| B、0.25 mol?L-1 |
| C、0.4 mol?L-1 |
| D、0.5 mol?L-1 |
25℃时,将a g硫酸铜晶体(CuSO4?5H2O)溶于b g水中,恰好形成V mL饱和溶液.下列关系正确的是( )
A、该饱和溶液硫酸铜物质的量浓度为 c=
| ||
B、该饱和溶液中硫酸铜的质量分数为ω=
| ||
C、25℃硫酸铜的溶解度为 S=
| ||
D、该饱和硫酸铜溶液的密度为 ρ=
|
下列说法正确的是( )
| A、同周期相邻主族的两元素原子序数均相差1 |
| B、原子最外层有2个电子的元素一定是金属元素 |
| C、第ⅦA族元素从上到下,其氢化物的酸性逐渐增强 |
| D、同主族元素从上到下,单质的熔点逐渐降低 |
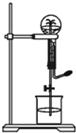 喷泉是一种常见的自然现象,其产生原因是存在压强差.图中为化学教学中所用的喷泉实验装置实验装置.已知3NO2+H2O=2HNO3+NO (NO为气体,难溶于水)在烧瓶中充满干燥NO2气体,胶头滴管及烧杯中分别盛有水进行喷泉实验.假设实验在标准状况下进行,经充分反应后,计算瓶内HNO3溶液的物质的量浓度为多少?
喷泉是一种常见的自然现象,其产生原因是存在压强差.图中为化学教学中所用的喷泉实验装置实验装置.已知3NO2+H2O=2HNO3+NO (NO为气体,难溶于水)在烧瓶中充满干燥NO2气体,胶头滴管及烧杯中分别盛有水进行喷泉实验.假设实验在标准状况下进行,经充分反应后,计算瓶内HNO3溶液的物质的量浓度为多少?