 最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂1mol N-N吸收167kJ热量,生成1mol N≡N放出942KJ,根据以上信息和数据,下列说法正确的是( )
最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂1mol N-N吸收167kJ热量,生成1mol N≡N放出942KJ,根据以上信息和数据,下列说法正确的是( )| A、N4属于一种新型的化合物 |
| B、N4与N2互为同位素 |
| C、N4与N2互为同素异形体 |
| D、1mol N4气体转变为N2将吸收882kJ热量 |
邻苯二甲醛(X)在碱性条件下发生歧化(即自身氧化还原)反应,再经酸化得到化合物Y.Y可在浓硫酸存在的条件下生成含五元环的化合物Z.则下列说法正确的是( )
| A、邻二甲苯不可用作生产X的原料 |
| B、Y可发生银镜反应 |
| C、Y可与FeCl3发生显色反应 |
| D、Z与X的相对分子质量相等 |
下列叙述正确的是( )
| A、晶体中只要有阳离子就一定有阴离子 |
| B、金刚石和冰在熔化时克服的作用力相同 |
| C、HCl晶体由H+和Cl-构成 |
| D、原子晶体里,所有原子都以共价键相互结合 |
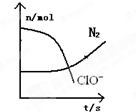 某容器中发生一个化学反应,反应过程中存在H2O、ClO-、CN-、HCO3-、N2、Cl-六种物质,在反应过程中测得ClO和N2的物质的量随时间变化的曲线如图所示.下列有关判断中正确的是( )
某容器中发生一个化学反应,反应过程中存在H2O、ClO-、CN-、HCO3-、N2、Cl-六种物质,在反应过程中测得ClO和N2的物质的量随时间变化的曲线如图所示.下列有关判断中正确的是( )| A、还原剂是CN-,氧化产物只有N2 |
| B、氧化剂是ClO-,还原产物是HCO3- |
| C、配平后氧化剂与还原剂的计量系数之比为5:2 |
| D、标准状况下若生成2.24LN2,则转移电子0.5 mol |
工业废气中的氮氧化物(如NO、NO2等,用通式NOx表示)是主要的大气污染物之一.为了保护环境,工业上常通入氨气与之发生如下反应:NOx+NH3-→N2+H2O来消除污染.有关此反应,下列说法中错误的是( )
| A、N2既是氧化产物又是还原产物 |
| B、当x=1时,每生成2.5 mol N2,被氧化的气体有3 mol |
| C、当x=2时,有1 mol气体被还原,转移电子4 mol |
| D、反应通式配平表示为:6NOx+4xNH3═(3+2x)N2+6xH2O |
对反应xR2++yH++O2=mR3++nH2O的离子方程式中,对m和R3+判断正确的是( )
| A、m=4,R3+是氧化产物 | ||
| B、m=y,R3+是还原产物 | ||
| C、m=2,R3+是氧化产物 | ||
D、m=
|
下列变化必须加入其他物质作还原剂才能发生的是( )
| A、CuO→CuCl2 |
| B、CO2→CO |
| C、HCl→Cl2 |
| D、H2O→H2 |
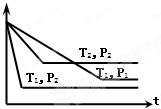 已知某可逆反应:mA(g)+nB(g)?xC(g),在密闭容器中进行,右图表示反应在不同时间t、温度T和压强P与C在混合气体中的百分含量(C%)的关系曲线,则正确的是( )
已知某可逆反应:mA(g)+nB(g)?xC(g),在密闭容器中进行,右图表示反应在不同时间t、温度T和压强P与C在混合气体中的百分含量(C%)的关系曲线,则正确的是( )| A、T1>T2,P1>P2,m+n>x,正反应放热 |
| B、T1<T2,P1<P2,m+n<x,正反应吸热 |
| C、T1>T2,P1<P2,m+n<x,正反应放热 |
| D、T1<T2,P1>P2,m+n>x,正反应吸热 |
已知常温下在溶液中可发生如下两个离子反应:①Ce4++Fe2+=Fe3++Ce3+②Sn2++2Fe3+=2Fe2++Sn4+ 下列说法正确的是( )
| A、反应②中的被还原与被氧化的离子的个数之比是1:2 |
| B、反应②中每2mol Fe3+参加反应转移1mol电子 |
| C、氧化性:Ce4+>Fe3+>Sn4+ |
| D、还原性:Fe2+>Ce3+>Sn2+ |