三氟化氮(NF3)是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3.则下列说法正确的是( )
| A、NF3是氧化剂,H2O是还原剂 |
| B、NF3是一种无色、无臭的气体,因此NF3在空气中泄漏时不易被察觉 |
| C、一旦NF3泄漏,可以用NaOH溶液喷淋的方法减少空气污染 |
| D、若生成0.2molHNO3,则转移0.2mol电子 |
下列说法中正确的是( )
| A、电子云示意图中的每个小黑点都表示一个电子 |
| B、镁原子的电子从基态跃迁到激发态,会释放能量 |
| C、s轨道电子能量一定比p轨道电子能量低 |
| D、氧原子核外有8种运动状态不同的电子 |
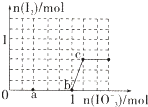 已知含3molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示,则下列判断不正确的是( )
已知含3molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示,则下列判断不正确的是( )| A、还原性:HSO3->I-,氧化性:IO3->I2>SO42- |
| B、a点处的氧化产物是SO42-,还原产物是I- |
| C、当溶液中的I-为0.4mol时,加入的KIO3一定为0.4mol |
| D、若向KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为:2IO3-+5HSO3-=I2,+5SO42-+3H++H2O |
现有A、B、C、D四种短周期元素,其中两种是金属元素.已知A、B同主族,B、C、D同周期,A、B的原子序数之和等于C、D的原子序数之和,C的单质能分别跟B和D的最高价氧化物的水化物反应.下列说法正确的是( )
| A、A的氢化物比B的氢化物难分解是因为A分子间能形成氢键 |
| B、含C元素的盐溶液一定呈酸性 |
| C、将a g C6H12O6在足量氧气中燃烧产物通入足量A和D按原子个数比1:1组成的化合物中,该化合物增重a g |
| D、D和A两元素形成的化合物,阴阳离子个数比分别为为1:1 和1:2 |
已知 ①2H2S+SO2═3S↓+2H2O ②2FeCl2+Cl2═2FeCl3
③2FeCl3+2HI═2FeCl2+2HCl+I2 ④I2+SO2+H2O═H2SO4+2HI
判断氧化性物质的氧化性由强到弱的顺序( )
③2FeCl3+2HI═2FeCl2+2HCl+I2 ④I2+SO2+H2O═H2SO4+2HI
判断氧化性物质的氧化性由强到弱的顺序( )
| A、Cl2>I2>FeCl3>SO2>S |
| B、Cl2>FeCl3>I2>SO2>S |
| C、Cl2>FeCl3>SO2>I2>S |
| D、FeCl3>Cl2>I2>SO2>S |
下列判断中一定正确的是( )
| A、若A2+2D-═2A-+D2,则还原性:D->A- |
| B、若R2+和M+的电子层结构相同,则碱性:ROH>MOH |
| C、若X2、Y2都是气态单质,且酸性HX>HY,元素原子得电子能力X>Y |
| D、若M、N是同主族元素,且原子序数:M>N,则元素原子得电子能力:M>N |
下列关于晶体与非晶体的说法不正确的是( )
| A、晶体具有固定的熔沸点 |
| B、晶体具有各向异性 |
| C、许多玻璃制品具有规则的几何外形,所以玻璃属于晶体 |
| D、区分晶体和非晶体最可靠的方法是对固体进行X-射线衍射实验 |
已知下列几个反应的化学方程式:下列有关物质的氧化性的强弱排列顺序中正确的是( )
①2KI+Cl2═2KCl+I2;
②2FeCl2+Cl2═2FeCl3;
③2FeCl3+2HI═2FeCl2+I2+2HCl;
④I2+SO2+2H2O═H2SO4+2HI.
①2KI+Cl2═2KCl+I2;
②2FeCl2+Cl2═2FeCl3;
③2FeCl3+2HI═2FeCl2+I2+2HCl;
④I2+SO2+2H2O═H2SO4+2HI.
| A、Cl2>Fe3+>I2>SO2 |
| B、Cl2>I2>Fe3+>SO2 |
| C、Cl2>Fe3+>SO2>I2 |
| D、Fe3+>I2>Cl2>SO2 |