题目内容
已知下列几个反应的化学方程式:下列有关物质的氧化性的强弱排列顺序中正确的是( )
①2KI+Cl2═2KCl+I2;
②2FeCl2+Cl2═2FeCl3;
③2FeCl3+2HI═2FeCl2+I2+2HCl;
④I2+SO2+2H2O═H2SO4+2HI.
①2KI+Cl2═2KCl+I2;
②2FeCl2+Cl2═2FeCl3;
③2FeCl3+2HI═2FeCl2+I2+2HCl;
④I2+SO2+2H2O═H2SO4+2HI.
| A、Cl2>Fe3+>I2>SO2 |
| B、Cl2>I2>Fe3+>SO2 |
| C、Cl2>Fe3+>SO2>I2 |
| D、Fe3+>I2>Cl2>SO2 |
考点:氧化性、还原性强弱的比较
专题:
分析:氧化还原反应中含有元素化合价降低的物质为氧化剂,通过氧化反应得到的产物为氧化产物,根据氧化还原反应中氧化剂的氧化性强于氧化产物的氧化性来解答.
解答:
解:①反应Cl2+2KI═I2+2KCl,氧化剂为Cl2,氧化产物为I2,所以氧化性Cl2>I2;
②2FeCl2+Cl2═2FeCl3,氧化剂为Cl2,氧化产物为FeCl3,所以氧化性Cl2>Fe3+;
③2FeCl3+2HI═I2+2FeCl2+2HCl,氧化剂为FeCl3,氧化产物为I2,所以氧化性Fe3+>I2;
④I2+SO2+2H2O═2HI+H2SO4,氧化剂为I2,还原剂是SO2,所以氧化性I2>SO2.
所以氧化性Cl2>Fe3+>I2>SO2.
故选A.
②2FeCl2+Cl2═2FeCl3,氧化剂为Cl2,氧化产物为FeCl3,所以氧化性Cl2>Fe3+;
③2FeCl3+2HI═I2+2FeCl2+2HCl,氧化剂为FeCl3,氧化产物为I2,所以氧化性Fe3+>I2;
④I2+SO2+2H2O═2HI+H2SO4,氧化剂为I2,还原剂是SO2,所以氧化性I2>SO2.
所以氧化性Cl2>Fe3+>I2>SO2.
故选A.
点评:本题考查了根据方程式来比较氧化性和还原性,解题的关键是根据化合价找出氧化剂、还原剂、氧化产物和还原产物,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列能说明可逆反应2A(g)+B(g)?2C(g)+D(g)在一定条件下已达到化学平衡状态的事实是( )
| A、容器内压强不随时间的变化而变化 |
| B、容器内A、B、C、D四者共存 |
| C、C的生成速率是D的生成速率的两倍 |
| D、A的消耗速率是D的消耗速率的两倍 |
常温下,下列各组粒子在指定溶液中能量共存的是( )
| A、在酸性KMnO4溶液中:Na+、C2H5OH、NH4+、Cl- |
| B、能溶解CaCO3的溶液中:Fe2+、Ca2÷、Cl-、NO3- |
| C、澄清透明的溶液中:Cu2+、Mg2+、SO42-、Cl- |
| D、能使淀粉-KIO3试纸显蓝色的溶液中:K+、H+、SO42-、I- |
下列对化学反应速率的认识正确的是( )
| A、H+和OH-的反应活化能接近于零,反应几乎在瞬间完成 |
| B、对于任何化学反应来说,反应速率越大,反应现象就越明显 |
| C、选用适当的催化剂,分子运动加快,增加了碰撞频率,故反应速率增大 |
| D、化学反应速率是指一定时间内任何一种反应物浓度的减少或任何一种生成物浓度的增加 |
下列描述中正确的是( )
| A、已知C(金刚石,s)=C(石墨,s)△H<0,则金刚石比石墨稳定 |
| B、CO(g)的燃烧热是283.0 kJ?mol-1,则2CO2(g)=2CO(g)+O2(g)的△H=2×(+283.0)kJ?mol-1 |
| C、HCl和NaOH反应的中和热△H=-57.3 kJ?mol-1,则H2SO4和Ba(OH)2的反应热△H=2×(-57.3)kJ?mol-1 |
| D、1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
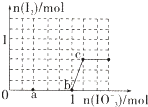 已知含3molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示,则下列判断不正确的是( )
已知含3molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示,则下列判断不正确的是( )| A、还原性:HSO3->I-,氧化性:IO3->I2>SO42- |
| B、a点处的氧化产物是SO42-,还原产物是I- |
| C、当溶液中的I-为0.4mol时,加入的KIO3一定为0.4mol |
| D、若向KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为:2IO3-+5HSO3-=I2,+5SO42-+3H++H2O |
3NO2十H2O═2HNO3十NO为工业上氨催化氧化法制硝酸的反应之一,该反应中NO2的作用是( )
| A、只作氧化剂 |
| B、作催化剂 |
| C、既作氧化剂又作还原剂 |
| D、作干燥剂 |
下列说法正确的是( )
| A、两种原子形成的共价键一定是极性共价键 |
| B、元素金属性越强,对应单质的还原性越强;元素非金属性越强,对应单质的氧化性越强 |
| C、由金属元素和非金属元素组成的化合物一定是离子化合物 |
| D、按照元素周期表的排布规律,非金属元素最多有23种 |
下列说法正确的是( )
| A、硫酸、纯碱、碳酸钠和生石灰分别属于酸、碱、盐和氧化物 |
| B、生石灰与水混合的过程只发生物理变化 |
| C、可用丁达尔效应区分溶液与胶体 |
| D、CuSO4?5H2O是一种混合物 |