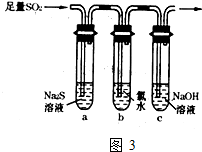
碘与氢气反应的热化学方程式是①I2(g)+H2(g)?2HI(g)△H=-9.48kJ?mol-1 ②I2(s)+H2(g?2HI(g)△H=+26.48kJ?mol-1下列说法正确的是( )
| A、从上述两反应可知1mol的I2(g)能量比1mol的I2(s)能量高 |
| B、I2(s)?I2(g)△H<0 |
| C、②的反应物总能量与①的反应物总能量相等 |
| D、1 mol I2(g)中通入1 mol H2(g),发生反应时放出的热量为9.48 kJ?mol-1 |
同主族元素所形成的同一类化合物,往往其结构和性质相似.化合物PH4I是一种无色晶体,下列对它的描述错误的是( )
| A、是一种共价化合物 |
| B、可由PH3与HI化合生成 |
| C、在加热的条件下,可以分解产生有色气体 |
| D、能跟碱反应放出PH3 |
已知化学反应A2(g)+B2(g)═2AB(g)△H=Q kJ?mol-1,其能量变化如图所示,则Q的值正确的是( )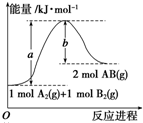

| A、a-b | B、a | C、-b | D、b-a |
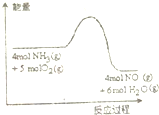 一定条件下密闭容器中发生如图反应:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)反应过程中能量变化如图所示,下列说法正确的是( )
一定条件下密闭容器中发生如图反应:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)反应过程中能量变化如图所示,下列说法正确的是( )| A、降低温度可以加快正反应速率 |
| B、反应体系中加入催化剂可增加反应热 |
| C、降低温度可以提高NH3的转化率 |
| D、增加空气的量可以提高混合气体中NO的体积分数 |
下列关于氯水的叙述,正确的是( )
| A、新制氯水中只含Cl2和H2O分子 |
| B、新制氯水可使蓝色石蕊试纸先变红后褪色 |
| C、光照氯水有气泡逸出,该气体是Cl2 |
| D、氯水放置数天后酸性下降 |
近期我国提出控制温室气体排放的措施和近期指标,旨在“善待地球--科学发展”.下列不符合这一主题的是( )
| A、发展循环经济,构建资源节约型社会 |
| B、加高工厂的烟囱,使烟尘和废气远离地表,减少污染 |
| C、减少直至不使用对大气臭氧层起破坏作用的氟氯烃 |
| D、采用“绿色化学”工艺,建立环境友好型化工体系 |
下列有关热化学方程式的叙述正确的是( )
| A、已知2H2(gO2(g)=2H2O(g);△H=-483.6 kJ/mol,则氢气的燃烧热为241.8 kJ/mol |
| B、已知C(石墨,s)=C(金刚石,s);△H>0,则金刚石比石墨稳定 |
| C、含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则该反应中和热的热化学方程式为:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(aq);△H=-57.4 kJ/mol |
| D、已知2C(s)+2O2(g)=2CO2(g);△H1,2C(s)+O2(g)=2CO(g);△H2.则△H1<△H2 |