下列各项中的事实能用同一原理解释的是( )
| A、明矾和氯水都用于自来水的处理 |
| B、.干冰和碘化银都可用于人工降雨 |
| C、向Fe(OH)3胶体和NaAlO2溶液中逐滴加盐酸,先出现沉淀,然后溶解 |
| D、铁器和铝制容器都可以用来运输浓硫酸 |
 常温下,向10mL 0.1mol?L-1 NaOH溶液中逐滴加入0.1mol?L-1的CH3COOH溶液,其pH逐渐减小,图中a、b、c三点的pH为实验中所测得.下列有关说法中一定正确的是( )
常温下,向10mL 0.1mol?L-1 NaOH溶液中逐滴加入0.1mol?L-1的CH3COOH溶液,其pH逐渐减小,图中a、b、c三点的pH为实验中所测得.下列有关说法中一定正确的是( )| A、当7<pH<13时,溶液中c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| B、当pH=7时,所加CH3COOH溶液的体积为10 mL |
| C、当5<pH<7时,溶液中c(CH3COO-)>c(Na+) |
| D、继续滴加0.1 mol?L-1的CH3COOH溶液,溶液的pH最终可以变化至1 |
室温时,盐酸和硫酸的混合溶液20ml,向混合溶液中逐滴加入0.05mol?L-1Ba(OH)2溶液时,生成的BaSO4和pH的变化如图所示(不考虑溶液混合时体积的变化).下列说法正确的是( )
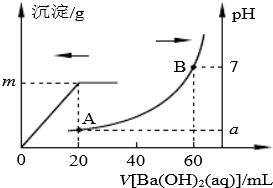

| A、图中A点对应溶液的pH=l |
| B、生成沉淀的最大质量m=2.33 g |
| C、原混合溶液中盐酸物质的量浓度为0.1 mol?L-1 |
| D、当V[Ba(OH)2(aq)]=10 mL时,发生反应的离子方程式为:Ba2++SO42-═BaSO4↓ |
向100mL的FeBr2溶液中通入标准状况下C123.36L,所得溶液中C1一和Br-的物质的量浓度相等,则原FeBr2溶液的物质的量浓度为( )
| A、0.75mol?L-1 |
| B、1 mol?L-1 |
| C、1.5 mol?L-1 |
| D、2 mol?L-1 |
有BaCl2和NaCl的混合溶液a L,将其分成两等份.一份滴加稀硫酸,使Ba2+完全沉淀,另一份滴加AgNO3溶液,使Cl-完全沉淀.反应中分别消耗b mol的H2SO4和c mol的AgNO3.据此得知原混合溶液中的Na+的物质的量浓度为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
 向甲、乙两恒温恒容的密闭容器中分别充入一定量的A和B,发生反应:
向甲、乙两恒温恒容的密闭容器中分别充入一定量的A和B,发生反应:A(g)+B(g)?xC(g)△H<O.测得两容器中c(A)随时间t的变化如图所示:下列说法正确的是( )
| 容器 | 甲 | 乙 |
| 容积(L) | 0.5 | 0.5 |
| 反应放热(kJ) | Q1 | Q2 |
| 反应物起始量 | 1molA 1molB | 0.5molA 0.5molB |
| A、x=1 |
| B、Q1<2Q2 |
| C、根据题中信息无法计算a值 |
| D、保持其他条件不变,起始时向乙容器充人0.2mol A、0.2mol B、0.2mol C,则此时v(正)>v(逆) |
生活中碰到的某些问题,常涉及到化学知识,下列分析不正确的是( )
| A、医疗上常用体积分数为70%~75%的酒精作消毒剂 |
| B、用灼烧并闻气味的方法区别纯棉织物和纯毛织物 |
| C、某酸雨样品采集后放置一段时间,pH值变小,是因为水中又溶解了较多的CO2 |
| D、为防止流感传染,可将教室门窗关闭后,用食醋熏蒸,进行消毒 |
能区别甲烷和乙烯两种气体的化学试剂是( )
| A、NaOH 溶液 |
| B、HCl |
| C、乙醇 |
| D、酸性高锰酸钾溶液 |
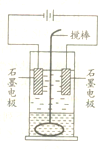 在玻璃圆筒中盛有两种无色的互不相溶的中性液体.上层液体中插有两根石墨电极,圆筒内还放有一根下端弯成环状的玻璃搅拌棒,可以上下搅动液体,装置如图所示.接通电源,阳极周围的液体呈棕色,且颜色由浅变深,阴极上有气泡生成.停止通电,取出电极,用搅棒上下剧烈搅动.静置后液体又分成两层,下层液体呈紫红色,上层液体几乎无色.回答:
在玻璃圆筒中盛有两种无色的互不相溶的中性液体.上层液体中插有两根石墨电极,圆筒内还放有一根下端弯成环状的玻璃搅拌棒,可以上下搅动液体,装置如图所示.接通电源,阳极周围的液体呈棕色,且颜色由浅变深,阴极上有气泡生成.停止通电,取出电极,用搅棒上下剧烈搅动.静置后液体又分成两层,下层液体呈紫红色,上层液体几乎无色.回答:

 ,参照上述合成路线中的有关信息,写出由对甲苯酚为原料合成
,参照上述合成路线中的有关信息,写出由对甲苯酚为原料合成 的合成流程图(其它试剂自选)
的合成流程图(其它试剂自选)