下列家庭化学小实验能达到预期目的是( )
| A、用米汤检验食用加碘盐(含KIO3)中含有碘 |
| B、用碘酒检验汽油中是否含有不饱和烃 |
| C、提纯蛋白质可以在蛋白质溶液中加饱和CuSO4溶液,蛋白质析出,然后把沉淀溶于蒸馏水中 |
| D、淀粉溶液中加入硫酸加热水解,冷却,加银氨溶液做银镜反应 |
下列试剂中,可将乙醇、淀粉溶液和苯三种无色液体鉴别开的是( )
| A、氢氧化钠 |
| B、新制Cu(OH)2浊液 |
| C、溴水 |
| D、碘水 |
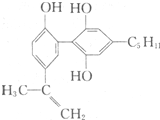 举办“人文奥运”的一个重要体现就是禁止运动员服用兴奋剂.有一种兴奋剂的结构简式如图,下列有关该物质的说法正确的是( )
举办“人文奥运”的一个重要体现就是禁止运动员服用兴奋剂.有一种兴奋剂的结构简式如图,下列有关该物质的说法正确的是( )| A、该分子中所有碳原子一定共存于同一平面中 |
| B、1 mol该物质与足量浓溴水反应时,至少消耗4 molBr2 |
| C、该物质属于苯酚同系物,则其遇FeCl3溶液一定显色 |
| D、由于该物质能使酸性KMn04溶液褪色,即可证明其分子必存在碳碳双键 |
1mol某有机物在稀硫酸作用下,水解生成2摩相同的物质.下列物质中:①蔗糖 ②麦芽糖 ③淀粉④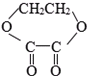 ⑤
⑤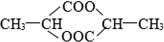 ⑥
⑥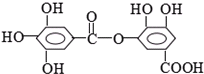
符合题意的物质可能是( )
 ⑤
⑤ ⑥
⑥
符合题意的物质可能是( )
| A、①②⑤ | B、②④⑤ |
| C、②⑤⑥ | D、①④⑤⑥ |
亚麻油酸是淡黄色的透明液体,在医疗上可用于治疗高血脂和动脉硬化,花生油中富含亚麻油酸,其结构简式为CH3(CH2)4CH=CHCH2CH=CH(CH2)7COOH,下列说法中正确的是( )
| A、亚麻油酸是一种酯类 |
| B、等物质的量的两份亚麻油酸分别和Na、H2反应,消耗二者的物质的量之比为1:1 |
| C、亚麻油酸可以发生氧化、加成、水解等反应 |
| D、亚麻油酸能使溴的CCl4溶液褪色 |
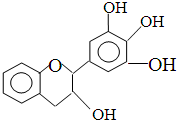 “茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中不正确的是( )
“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中不正确的是( )| A、遇FeCl3溶液发生显色反应 |
| B、1molEGC与3molNaOH恰好完全反应 |
| C、易发生氧化反应和取代反应,难发生加成反应 |
| D、分子中所有的原子共面 |
某有机物的结构简式为: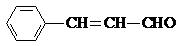 ,则关于该有机物的说法正确的是( )
,则关于该有机物的说法正确的是( )
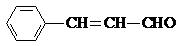 ,则关于该有机物的说法正确的是( )
,则关于该有机物的说法正确的是( )| A、1 mol该有机物发生银镜反应能生成 1 mol Ag |
| B、1 mol该有机物最多能够与6 mol H2 发生加成反应 |
C、它与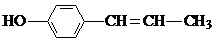 互为同分异构体 互为同分异构体 |
| D、该有机物能被酸性高锰酸钾溶液氧化 |

 金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀等性质被广泛用在高新科技材料和航天领域中.“硫酸法”生产钛的原料是钛铁矿(主要成分是:FeTiO3,还含有少量Mn、Zn、Cr、Cu等重金属元素及脉石等杂质);主要生产流程如下:
金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀等性质被广泛用在高新科技材料和航天领域中.“硫酸法”生产钛的原料是钛铁矿(主要成分是:FeTiO3,还含有少量Mn、Zn、Cr、Cu等重金属元素及脉石等杂质);主要生产流程如下: