题目内容
在一容积为4L的密闭容器中,加入0.4mol的N2和1.2mol的H2在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g )△H<0,反应中NH3的物质的量浓度变化情况如图1:
(1)根据如图1,计算从反应开始到平衡时,平均反应速率v(NH3)为 mol/(L?min).
(2)该反应的化学平衡常数表达式K ,随温度的升高,K值将 (填“增大”、“减小”“不变”)
(3)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为 .
a.0.20mol/L b.0.12mol/Lc.0.10mol/L d.0.08mol/L
(4)反应达到平衡后,第5分钟末,保持其它条件不变,若只把容器的体积缩小一半,平衡 移动(填“向逆反应方向”、“向正反应方向”或“不”),化学平衡常数 (填“增大”、“减小”或“不变”).
(5)在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25mol/L),请在如图1中画出第5分钟末到此平衡时NH3浓度的变化曲线.
(6)在三个相同容器中各充入1molN2和3molH2,在某一不同条件下反应并达到平衡,氨的体积分数随时间变化曲线如图2.下列说法正确的是 (填序号).
.图Ⅰ可能是不同压强对反应的影响,且P2>Pl
B.图Ⅱ可能是不同压强对反应的影响,且Pl>P2
C.图Ⅲ可能是不同温度对反应的影响,且T1>T2
D.图Ⅱ可能是同温同压下,催化剂性能,1>2.

(1)根据如图1,计算从反应开始到平衡时,平均反应速率v(NH3)为
(2)该反应的化学平衡常数表达式K
(3)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为
a.0.20mol/L b.0.12mol/Lc.0.10mol/L d.0.08mol/L
(4)反应达到平衡后,第5分钟末,保持其它条件不变,若只把容器的体积缩小一半,平衡
(5)在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25mol/L),请在如图1中画出第5分钟末到此平衡时NH3浓度的变化曲线.
(6)在三个相同容器中各充入1molN2和3molH2,在某一不同条件下反应并达到平衡,氨的体积分数随时间变化曲线如图2.下列说法正确的是
.图Ⅰ可能是不同压强对反应的影响,且P2>Pl
B.图Ⅱ可能是不同压强对反应的影响,且Pl>P2
C.图Ⅲ可能是不同温度对反应的影响,且T1>T2
D.图Ⅱ可能是同温同压下,催化剂性能,1>2.

考点:物质的量或浓度随时间的变化曲线,化学平衡常数的含义,化学平衡的影响因素
专题:
分析:(1)由图可知,4min 时反应达到平衡状态,达到平衡时氨气增加0.10mol/L,根据反应速率公式v=
计算氨气的反应速率;
(2)化学平衡常数K等于生成物浓度幂之积与反应物浓度幂之积的比,反应N2(g)+3H2(g)?2NH3(g )△H<0正反应为放热反应;
(3)根据反应的可逆性特点以及温度改变平衡一定发生移动进行判断;
(4)体积减小,气体压强增大,平衡向气体体积减小的方向移动,化学平衡常数只与温度有关,温度不变,化学平衡常数不变;
(5)第5分钟末将容器的体积缩小一半后,压强增大,平衡正向移动,氨气的浓度增大,在第8分钟末达到新的平衡时NH3的浓度约为0.25mol?L-1;
(6)A.增大压强平衡右移;
B.压强不同,平衡状态不同;
C.升高温度平衡逆向移动;
D.催化剂不影响平衡移动.
| △c |
| △t |
(2)化学平衡常数K等于生成物浓度幂之积与反应物浓度幂之积的比,反应N2(g)+3H2(g)?2NH3(g )△H<0正反应为放热反应;
(3)根据反应的可逆性特点以及温度改变平衡一定发生移动进行判断;
(4)体积减小,气体压强增大,平衡向气体体积减小的方向移动,化学平衡常数只与温度有关,温度不变,化学平衡常数不变;
(5)第5分钟末将容器的体积缩小一半后,压强增大,平衡正向移动,氨气的浓度增大,在第8分钟末达到新的平衡时NH3的浓度约为0.25mol?L-1;
(6)A.增大压强平衡右移;
B.压强不同,平衡状态不同;
C.升高温度平衡逆向移动;
D.催化剂不影响平衡移动.
解答:
解:(1)由图可知,达到平衡时氨气增加0.10mol/L,其反应速率v=
=
=0.025 mol?L-1?min-1,故答案为:0.025;
(2)该反应的化学平衡常数K=
,反应N2(g)+3H2(g)?2NH3(g )△H<0正反应为放热反应,随温度的升高,平衡逆向移动,平衡常数减小,故答案为:
;减小;
(3)该反应为可逆反应,反应物不可能完全转化,则NH3的物质的量浓度不可能为0.2mol/L,温度改变平衡一定发生移动,则NH3的物质的量浓度不可能为0.1mol/L,故答案为:a、c;
(4)该反应是气体体积减小的反应,把容器的体积缩小一半,增大了反应体系的压强,增大压强,平衡向气体体积减小的方向移动,即向正反应方向移动;化学平衡常数只与温度有关,温度不变,平衡常数不变,
故答案为:向正反应方向;不变;
(5)第5分钟末将容器的体积缩小一半后,氨气浓度为0.40mol/L,压强增大,平衡正向移动,氨气的浓度增大,在第8分钟末达到新的平衡时NH3的浓度约为0.50mol?L-1,则图象为 ,故答案为:
,故答案为: ;
;
(6)A.增大压强平衡右移,氨气的含量应增大,故A错误;
B.压强不同,平衡状态不同,不可能在同一平衡状态,故B错误;
C.升高温度平衡逆向移动,氨气的含量减小,故C错误;
D.催化剂不影响平衡移动,由图象可知催化剂性能,1>2,故D正确.
故答案为:D.
| △c |
| △t |
| 0.1mol/L |
| 4min |
(2)该反应的化学平衡常数K=
| c2(NH3) |
| c(N2)?c3(H2) |
| c2(NH3) |
| c(N2)?c3(H2) |
(3)该反应为可逆反应,反应物不可能完全转化,则NH3的物质的量浓度不可能为0.2mol/L,温度改变平衡一定发生移动,则NH3的物质的量浓度不可能为0.1mol/L,故答案为:a、c;
(4)该反应是气体体积减小的反应,把容器的体积缩小一半,增大了反应体系的压强,增大压强,平衡向气体体积减小的方向移动,即向正反应方向移动;化学平衡常数只与温度有关,温度不变,平衡常数不变,
故答案为:向正反应方向;不变;
(5)第5分钟末将容器的体积缩小一半后,氨气浓度为0.40mol/L,压强增大,平衡正向移动,氨气的浓度增大,在第8分钟末达到新的平衡时NH3的浓度约为0.50mol?L-1,则图象为
 ,故答案为:
,故答案为: ;
;(6)A.增大压强平衡右移,氨气的含量应增大,故A错误;
B.压强不同,平衡状态不同,不可能在同一平衡状态,故B错误;
C.升高温度平衡逆向移动,氨气的含量减小,故C错误;
D.催化剂不影响平衡移动,由图象可知催化剂性能,1>2,故D正确.
故答案为:D.
点评:本题考查化学平衡的计算,明确反应速率计算、平衡的影响因素及图象的分析试剂解答本题的关键,题目难度中等,难点是(5)题图象,注意缩小体积瞬间,氨气浓度变为原来的2倍,为易错点.

练习册系列答案
相关题目
亚麻油酸是淡黄色的透明液体,在医疗上可用于治疗高血脂和动脉硬化,花生油中富含亚麻油酸,其结构简式为CH3(CH2)4CH=CHCH2CH=CH(CH2)7COOH,下列说法中正确的是( )
| A、亚麻油酸是一种酯类 |
| B、等物质的量的两份亚麻油酸分别和Na、H2反应,消耗二者的物质的量之比为1:1 |
| C、亚麻油酸可以发生氧化、加成、水解等反应 |
| D、亚麻油酸能使溴的CCl4溶液褪色 |
环境污染已成为人类社会面临的重大威胁,各种污染数不胜数,下列各项中与环境污染无关的是( )
①家装中释放的甲醛 ②赤潮 ③酸雨 ④臭氧空洞 ⑤水俣病 ⑥大脖子病 ⑦水华 ⑧潮汐.
①家装中释放的甲醛 ②赤潮 ③酸雨 ④臭氧空洞 ⑤水俣病 ⑥大脖子病 ⑦水华 ⑧潮汐.
| A、①② | B、③④ | C、⑤⑥ | D、⑥⑧ |
下列离子在溶液中能大量共存的是( )
| A、HCO3-、Ba2-、SO42-、H+ |
| B、K+、SiO32-、H+、Cl- |
| C、Fe3+、OH-、NO3-、HCO3- |
| D、Al3+、H+、NO3-、SO42- |
下列实验方案不可行的是( )
| A、用稀盐酸清洗做焰色反应的铂丝 |
| B、金属钠保存在煤油中 |
| C、用湿润的淀粉KI试纸靠近试剂瓶口检验Cl2是否收集满 |
| D、除去粗盐溶液中的Ca2+、SO42-:先加Na2CO3溶液后加BaCl2溶液 |
下列各组混合物中,无论以何种比例混合,取nmol使之充分燃烧,耗氧量为定值的是( )
| A、C2H2、C2H4O |
| B、C2H4、C3H6 |
| C、C2H4、C2H6O |
| D、C6H12O6、C2H4O2 |
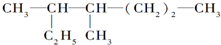 的名称是
的名称是