设NA为阿伏加德罗常数,下列说法中正确的是( )
| A、标准状况下4.48LH2O的分子个数为2NA |
| B、22克CO2的分子个数为0.5NA |
| C、1L浓度为0.1mol/L的MgCl2溶液中Cl-为0.1NA |
| D、标准状况下2.24LNO2中原子个数为0.2NA |
用NA表示阿伏德罗常数,下列叙述正确的是( )
| A、标准状况下,22.4LH2O含有的分子数为1 NA |
| B、32克氧气所含原子数目为4 NA |
| C、1 mol Ca变成Ca2+时失去的电子数为2NA |
| D、1 L 0.1mol?L-1 Na2SO4溶液中有0.1 NA个Na+ |
某一反应物的浓度为1.0mol/L,经过20s后,它的浓度变成了0.2mol/L,在这20s内它的反应速率为( )
| A、0.04 |
| B、0.04mol/L |
| C、0.04mol/(L?S) |
| D、0.8mol/(L?S) |
下列有关阿佛加德罗常数(NA)的说法错误的是( )
| A、32克O2所含的原子数目为2NA |
| B、0.5L 0.2mol/L的NaCl(aq)中含有的Na+数是0.1NA |
| C、标准状况下,22.4L水中含有NA个水分子 |
| D、0.5NA个氯气分子的物质的量是0.5mol |
下列有关化学用语使用正确的是:( )
①甲基环戊烷、聚丙烯的实验式均为CH2;
②氢氧根的电子式为: ;
;
③CH2=C(CH2CH3)2的名称为:2-乙基丁烯;
④丙烯的键线式为: ;
;
⑤α-羟基丙酸的比例模型为: ;
;
⑥3-甲基-1-硝基苯的结构简式为: .
.
①甲基环戊烷、聚丙烯的实验式均为CH2;
②氢氧根的电子式为:
 ;
;③CH2=C(CH2CH3)2的名称为:2-乙基丁烯;
④丙烯的键线式为:
 ;
;⑤α-羟基丙酸的比例模型为:
 ;
;⑥3-甲基-1-硝基苯的结构简式为:
 .
.| A、①、②、③ |
| B、①、②、⑤ |
| C、①、③、④ |
| D、②、④、⑥ |
埋在地下的自来水管,在下列情况下被腐蚀的速度最慢的是( )
| A、在含有铁元素的较多的酸性土壤中 |
| B、在潮湿、疏松的土壤中 |
| C、在自来水的铁管上用导线连接一块锌片后,再埋入不透气的土壤中 |
| D、在自来水的铁管上用导线连接一块铜片后,再埋入潮湿、疏松的土壤中 |
下列有关化学用语使用正确的是( )
A、醛基的电子式: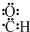 |
B、CH4Si的结构式: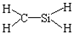 |
C、3,3-二甲基-1-戊烯的键线式: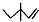 |
D、硝基苯的结构简式: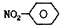 |
下列说法正确是的( )
| A、常温常压下,22.4L氖气含有NA个氖原子 |
| B、1molNa2O2固体跟足量CO2的气体完全反应转移NA个电子 |
| C、将CO2通入漂白粉溶液中一定有沉淀生成 |
| D、焰色反应属于化学变化 |
下列有关物质的性质与应用不相对应的是( )
| A、SO2具有氧化性,可用于漂白纸浆 |
| B、明矾能水解生成Al (OH)3胶体,可用作净水剂 |
| C、FeCl3溶液能与Cu反应,可用于蚀刻印刷电路 |
| D、Zn具有还原性和导电性,可用作锌锰干电池的负极材料 |