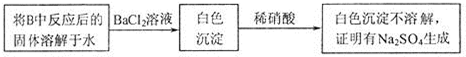
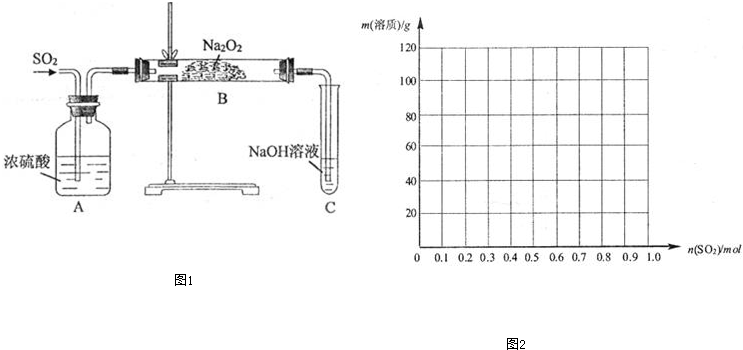
题目内容
设NA为阿伏加德罗常数,下列说法中正确的是( )
| A、标准状况下4.48LH2O的分子个数为2NA |
| B、22克CO2的分子个数为0.5NA |
| C、1L浓度为0.1mol/L的MgCl2溶液中Cl-为0.1NA |
| D、标准状况下2.24LNO2中原子个数为0.2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、标准状况下,水是液体,不能用气体摩尔体积计算物质的量;
B、22克CO2的物质的量为0.5mol,分子个数为0.5NA;
C、1L浓度为0.1mol/L的MgCl2溶液中Cl-为0.2NA;
D、标准状况下计算NO2物质的量n=
=
=0.1mol.
B、22克CO2的物质的量为0.5mol,分子个数为0.5NA;
C、1L浓度为0.1mol/L的MgCl2溶液中Cl-为0.2NA;
D、标准状况下计算NO2物质的量n=
| V |
| 22.4 |
| 2.24L |
| 22.4L/mol |
解答:
解:A、标准状况下,水是液体,不能用气体摩尔体积计算物质的量,故A错误;
B、22克CO2的物质的量为0.5mol,分子个数为0.5NA,故B正确;
C、1L浓度为0.1mol/L的MgCl2溶液中Cl-为0.2NA,故C错误;
D、标准状况下计算NO2物质的量n=
=
=0.1mol,NO2中原子个数为0.3NA,故D错误;
故选C.
B、22克CO2的物质的量为0.5mol,分子个数为0.5NA,故B正确;
C、1L浓度为0.1mol/L的MgCl2溶液中Cl-为0.2NA,故C错误;
D、标准状况下计算NO2物质的量n=
| V |
| 22.4 |
| 2.24L |
| 22.4L/mol |
故选C.
点评:本题考查了阿伏伽德罗常数的分析应用,主要是物质结构分析,分子、原离子,注意气体摩尔体积的应用,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
下列说法正确的是( )
| A、pH<7的溶液一定显酸性 |
| B、25℃时,pH=5的溶液与pH=3的溶液相比,前者c(OH-)是后者的100倍 |
| C、室温下,每1×107个水分子中只有一个水分子发生电离 |
| D、在0.1mol/L的氨水中,改变外界条件使c(NH4+)增大,则溶液的pH一定增大 |
埋在地下的自来水管,在下列情况下被腐蚀的速度最慢的是( )
| A、在含有铁元素的较多的酸性土壤中 |
| B、在潮湿、疏松的土壤中 |
| C、在自来水的铁管上用导线连接一块锌片后,再埋入不透气的土壤中 |
| D、在自来水的铁管上用导线连接一块铜片后,再埋入潮湿、疏松的土壤中 |
下列反应的离子方程式正确的是( )
| A、碳酸氢钙溶液中加入足量的苛性钠溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O | ||||
B、电解饱和食盐水:2Cl-+2H2O
| ||||
| C、氯气通入冷的氢氧化钠溶液中:2Cl2+2OH-=3Cl-+ClO-+H2O | ||||
| D、FeBr2溶液中通入足量的Cl2:2Fe2++Cl2=2Fe3++2Cl- |
下列反应的离子方程式书写正确的是( )
| A、过量氯气通入溴化亚铁溶液中:3Cl2+2Fe2++4Br-═6Cl-+2Fe3++2Br2 |
| B、在硫酸铜溶液中加入过量氢氧化钡溶液:Ba2++SO42-═BaSO4↓ |
| C、次氯酸钠溶液中通入二氧化硫气体:2ClO-+SO2+H2O═2HClO+SO32- |
| D、用稀硝酸除银镜:Ag+2H++NO3-═Ag++NO2↑+H2O |
下列有关氯的说法错误的是( )
| A、氯水、液氯中均含有Cl2分子,故两者均可显黄绿色 |
| B、氯水光照射时有气泡逸出,该气体的主要成分是氯气 |
| C、Cl2可以使湿润的有色布条褪色,是因为HClO有漂白性 |
| D、新制的氯水中分子由多到少的顺序是:H2O>Cl2>HClO |
高分子化合物
 是由下列加聚生成( )
是由下列加聚生成( )
①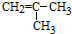 ②CH2═CH-CH═CH2③CH≡CH④CH3-CH═CH-CH3⑤
②CH2═CH-CH═CH2③CH≡CH④CH3-CH═CH-CH3⑤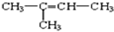
⑥CH3-CH2-CH═CH2.
 是由下列加聚生成( )
是由下列加聚生成( )①
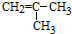 ②CH2═CH-CH═CH2③CH≡CH④CH3-CH═CH-CH3⑤
②CH2═CH-CH═CH2③CH≡CH④CH3-CH═CH-CH3⑤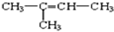
⑥CH3-CH2-CH═CH2.
| A、①②⑥ | B、①③⑤ |
| C、①②⑤ | D、②③⑤ |