题目内容
用NA表示阿伏德罗常数,下列叙述正确的是( )
| A、标准状况下,22.4LH2O含有的分子数为1 NA |
| B、32克氧气所含原子数目为4 NA |
| C、1 mol Ca变成Ca2+时失去的电子数为2NA |
| D、1 L 0.1mol?L-1 Na2SO4溶液中有0.1 NA个Na+ |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.气体摩尔体积只适用气体;
B.质量换算物质的量结合氧气分子式计算原子数;
C.钙原子最外层电子数为2,失去最外层电子析出钙离子;
D.依据n=CV计算硫酸钠的物质的量,1个硫酸钠电离产生2个钠离子.
B.质量换算物质的量结合氧气分子式计算原子数;
C.钙原子最外层电子数为2,失去最外层电子析出钙离子;
D.依据n=CV计算硫酸钠的物质的量,1个硫酸钠电离产生2个钠离子.
解答:
解:A.标况下,水为液体,不能使用气体摩尔体积,故A错误;
B.32克O2物质的量为1mol,所含的原子数目为2NA,故B错误;
C.钙原子最外层电子数为2,失去最外层电子变为钙离子,1 mol Ca变成Ca2+时失去的电子数为2NA,故C正确;
D.1个硫酸钠电离产生2个钠离子,1 L 0.1mol?L-1 Na2SO4溶液,硫酸钠的物质的量=1 L×0.1mol?L-1=0.1mol,含有钠离子个数为0.2NA,故D错误;
故选:C.
B.32克O2物质的量为1mol,所含的原子数目为2NA,故B错误;
C.钙原子最外层电子数为2,失去最外层电子变为钙离子,1 mol Ca变成Ca2+时失去的电子数为2NA,故C正确;
D.1个硫酸钠电离产生2个钠离子,1 L 0.1mol?L-1 Na2SO4溶液,硫酸钠的物质的量=1 L×0.1mol?L-1=0.1mol,含有钠离子个数为0.2NA,故D错误;
故选:C.
点评:本题考查阿伏加德罗常数的有关计算和判断,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,要准确弄清分子、原子、原子核内质子中子及核外电子的构成关系是解题关键,注意标况下的气体摩尔体积的使用条件,题目难度不大.

练习册系列答案
相关题目
下列操作中,能使电离平衡H2O?H++OH-向右移动且溶液呈酸性的是( )
| A、向水中加入NaHSO4溶液 |
| B、将水加热到100℃,使pH=6 |
| C、向水中加入Al2(SO4)3固体 |
| D、向水中加入CH3COONa固体 |
下列物质中,既能跟盐酸反应,又能跟氢氧化钠溶液反应的是( )
| A、Na2CO3 |
| B、NaHCO3 |
| C、Fe2O3 |
| D、CO2 |
mg铁粉与含有H2SO4的CuSO4溶液完全反应后,得到mg铜,则参与反应的CuSO4与H2SO4的物质的量之比为( )
| A、7:1 | B、1:7 |
| C、7:8 | D、8:7 |
下列有关化学用语使用正确的是( )
A、醛基的电子式: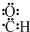 |
B、CH4Si的结构式: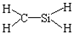 |
C、3,3-二甲基-1-戊烯的键线式: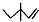 |
D、硝基苯的结构简式: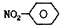 |
下列物质之间的反应,属于吸热反应的是( )
| A、Al和盐酸 |
| B、NaOH和H2SO4 |
| C、Ba(OH)2?8H2O和NH4Cl |
| D、Na2O2和H2O |
下列离子方程式正确的是( )
| A、二氧化硅与强碱溶液反应:SiO2+2OH-=SiO32-+H2O |
| B、将氯气通入水中:Cl2+H2O=2H++Cl-+ClO- |
| C、金属钠与水反应:Na+H2O=Na++OH-+H2↑ |
| D、少量的金属锌加入到FeCl3溶液中:2Fe3++3Zn=2Fe+3Zn2+ |
