盖斯定律在生产和科学研究中有很重要的作用,有些反应的反应热虽然无法直接测得,但可以利用盖斯定律间接计算求得.已知7.2g碳在12.8g的氧气中燃烧,至反应物耗尽,放出x kJ热量.已知单质碳的燃烧热为y kJ?mol-1,则1mol C与O2反应生成CO的反应热△H为( )
| A、-(2.5x-0.5 y) kJ?mol-1 |
| B、-(5x-0.5y) kJ?mol-1 |
| C、-(10x-y)kJ?mol-1 |
| D、-y kJ?mol-1 |
在无色透明的溶液中可以大量共存的离子组是( )
| A、H+、K+、Fe2+、NO3- |
| B、OH-、Cl-、Na+、NH4+ |
| C、Mg2+、K+、Cl-、NO3- |
| D、I-、Cl-、H+、Fe3+ |
已知反应3Cl2+6NaOH=5NaCl+NaClO3+3H2O下列说法正确的是( )
| A、Cl2既是氧化剂也是还原剂 |
| B、该反应中的电子转移数目为6e- |
| C、氧化剂和还原剂的质量比是1:5 |
| D、NaCl是氧化产物,NaClO3是还原产物 |
使石蕊试液变红的某透明溶液中,下列各组离子能大量共存的是( )
| A、CO32-、Na+、K+、OH- |
| B、Ba2+、CO32-、NO3-、SO42- |
| C、K+、Cu2+、Cl-、SO42- |
| D、Fe2+、NO3-、Cl-、SO42- |
室温下,pH等于2的CH3COOH溶液与pH=12的NaOH溶液等体积混合,则混合后溶液的pH值为( )
| A、大于7或等于7 |
| B、小于7 |
| C、小于7或等于7 |
| D、无法确定 |
向某密闭容器中加入0.3molA,0.1molC和一定量的B三种气体在一定条件下发生反应,各物质浓度随时间变化如甲图所示[t0~tl阶段的c(B)变化未画出].乙图为t2时刻后改变条件平衡体系中正、逆反应速率随时间变化的情况,且四个阶段都各改变一种反应条件(浓度、温度、压强、催化剂)且互不相同,t3~t4阶段为使用催化剂.下列说法中正确的是( )
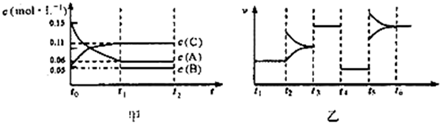

| A、其他条件不变时,增大压强,B的转化率不变 |
| B、t4~t5阶段改变的条件为降低温度 |
| C、B的起始物质的量为0.02mol |
| D、若t5~t6阶段改变的条件为升高温度,则正反应为吸热反应 |
海洋中有丰富的食品、矿产、能源、药物和水产资源,如图为海水利用的部分过程.下列有关说法正确的是( )


| A、制取NaHCO3的反应是利用其溶解度小于NaCl |
| B、用澄清的石灰水可鉴别NaHCO3溶液和Na2CO3溶液 |
| C、在第③、④、⑤步骤中,溴元素均被氧化 |
| D、加热MgCl2溶液制取无水氯化镁 |
将充有mmLNO和nmLNO2的量筒倒立于水槽中,然后通入mmLO2,若m<n,则充分反应后量筒内气体体积(mL)为( )
| A、3(m-n) | ||
B、
| ||
C、
| ||
D、
|
2011年1月14日,我国材料科学的一代宗师师昌绪,荣获2010年度中国科技界的最高荣誉“国家最高科学技术奖”,他主要从事高温合金及高合金钢研究,领导研制出我国第一代空心气冷铸造镍基高温合金涡轮叶片等多项成果,下列关于合金的叙述正确的是( )
| A、合金的熔点一般比组分金属高 |
| B、合金中只含金属元素 |
| C、合金的机械性能一般比组分金属好 |
| D、合金不容易发生电化学腐蚀 |
生铁的熔点是1100℃~1200℃,则纯铁的熔点可能是( )
| A、1055℃ |
| B、1100℃ |
| C、1200℃ |
| D、1535℃ |