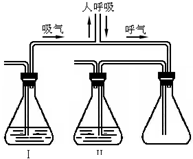
 某化学兴趣小组为了证明人呼出的气体中含有CO2,设计了如图所示的实验装置.你认为锥形瓶Ⅰ、Ⅱ中应选用的一组试剂是( )
某化学兴趣小组为了证明人呼出的气体中含有CO2,设计了如图所示的实验装置.你认为锥形瓶Ⅰ、Ⅱ中应选用的一组试剂是( )| A. | B. | C. | D. | |
| 瓶Ⅰ | KOH | NaOH | 稀HCl | Na2SO4 |
| 瓶Ⅱ | NaOH | Ca(OH)2 | AgNO3 | BaCl2 |
| A、A | B、B | C、C | D、D |
 某化学兴趣小组为了证明人呼出的气体中含有CO2,设计了如图所示的实验装置.你认为锥形瓶Ⅰ、Ⅱ中应选用的一组试剂是( )
某化学兴趣小组为了证明人呼出的气体中含有CO2,设计了如图所示的实验装置.你认为锥形瓶Ⅰ、Ⅱ中应选用的一组试剂是( )| A. | B. | C. | D. | |
| 瓶Ⅰ | KOH | NaOH | 稀HCl | Na2SO4 |
| 瓶Ⅱ | NaOH | Ca(OH)2 | AgNO3 | BaCl2 |
| A、A | B、B | C、C | D、D |