水的电离平衡曲线如图所示,下列说法不正确的是( )
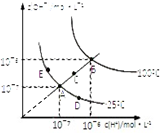

| A、图中五点KW间的关系:B>C>A=D=E |
| B、若从A点到D点,可采用:温度不变时在水中加入少量酸 |
| C、在B点对应的温度下,将pH=2的硝酸与pH=10的Ba(OH)2(aq)等体积混合后,溶液显中性 |
| D、若从A点到C点,可采用:温度不变时在水中加入适量的NH4Cl固体 |
对含有酚酞的下列溶液操作后颜色变深的是( )
| A、AlCl3溶液中再溶入AlCl3 |
| B、CH3COONa稀溶液加热 |
| C、氨水中加入少量NH4Cl固体 |
| D、醋酸溶液加热 |
在室温下pH=13的强碱与pH=2的强酸溶液混合,所得混合液的pH=11,则强碱与强酸的体积比为( )
| A、9:1 | B、1:11 |
| C、1:9 | D、11:1 |
在室温下,等体积的酸和碱的溶液,混合后pH一定等于7的是( )
| A、同浓度的H2SO4溶液于KOH溶液 |
| B、pH=3的盐酸和pH=11的氨水 |
| C、pH=3的硫酸和pH=11的KOH |
| D、pH=3的醋酸和pH=11的KOH溶液 |
下列电解质溶液的有关叙述正确的是( )
| A、在CH3COONa溶液中加入适量CH3COOH,可使c(Na+)=c(CH3COO-) |
| B、pH=3的CH3COOH与pH=11的NaOH溶液等体积混合后,溶液显碱性 |
| C、将足量CuSO4溶液在0.1mol?L-1的H2S溶液中,Cu2+能达到的最大浓度为1.3×10-35mol?L-1(已知:Ksp(CuS)=1.3×10-36) |
| D、含1molKOH的溶液与1molCO2完全反应后,溶液中c(K+)=c(HCO3-) |
在一定条件下发生下列反应,其中属于盐类水解反应的是( )
| A、HS-+H+═H2S |
| B、HCO3-+H2O?H3O++CO32- |
| C、NH4++H2O?NH3?H2O+H+ |
| D、Cl2+H2O?H++Cl-+HClO |
下列式子中,属于水解反应的是( )
| A、H2O+H2O?H3O++OH- |
| B、CO32-+H2O?HCO3-+OH- |
| C、NH3+H2O?NH3.H2O |
| D、HCO3-+OH-?H2O+CO32- |
对于某些离子的检验及结论一定正确的是( )
| A、加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,有CO32-或HCO3-中的一种或两种 |
| B、加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- |
| C、加入硝酸酸化的硝酸银溶液有白色沉淀生成,则溶液中一定含有Cl- |
| D、加入碳酸钠溶液产生白色沉淀,再加盐酸,白色沉淀消失,一定有Ba2+ |
对于0.1mol/L Na2CO3溶液,下列说法正确的是( )
| A、升高温度,溶液的pH降低 |
| B、c(Na+)=2c(CO32-)+c(HCO3-)+c(H2CO3) |
| C、加入少量NaOH固体,c(CO32-)与c(Na+)均增大 |
| D、c(Na+)+c(H+)=2c(CO32-)+2c(HCO3-)+c(OH-) |
下列溶液显酸性的是( )
| A、NaCl溶液 |
| B、Na2CO3溶液 |
| C、AlCl3溶液 |
| D、KNO3溶液 |