阿波罗宇宙飞船上使用的是氢氧燃料电池,其电池总反应式为:2H2+O2=2H2O,电解液为KOH溶液,反应保持在较高温度使水蒸发,下列叙述中正确的是( )
| A、工作时,电解质溶液的pH逐渐增大 |
| B、工作时,能见到浅蓝色火焰 |
| C、工作时,H2为正极,O2为负极 |
| D、电极反应式为:负极:2H2+4OH--4e-=4H2O正极:O2+2H2O+4e-=4OH- |
下列有关防护金属腐蚀的说法中,不正确的是( )
| A、青铜(锡铜合金)中的锡可对铜起保护作用 |
| B、在海轮外壳上焊接上锌块,可减缓船体的腐蚀速率 |
| C、海水中钢闸门与电源的正极相连,可以防止闸门的腐蚀 |
| D、钢铁表面烤蓝生成一层致密的Fe3O4,能起到防腐蚀的作用 |
24mL 0.05mol/L的Na2SO3溶液,恰好与20mL 0.02mol/L的K2Cr2O7溶液完全反应,已知Na2SO3被氧化为Na2SO4,则元素Cr在被还原的产物中的化合价是( )
| A、+2 | B、+3 | C、+4 | D、+5 |
下列说法中正确的是( )
| A、凡是放热反应都是自发的,凡是吸热反应都是非自发的 |
| B、自发反应熵一定增大,非自发反应熵一定减小或不变 |
| C、要判断反应进行的方向,必须综合考虑体系的焓变和熵变 |
| D、自发反应在任何条件下都能实现 |
下列各项表达中正确的是( )
A、-CH3(甲基)的电子式: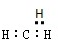 |
B、硝基苯的结构简式: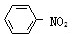 |
C、甲醛的结构式: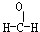 |
D、聚丙烯的结构简式: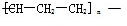 |
在一密闭烧瓶中,在25℃时存在如下平衡:2NO2(g)?N2O4(g)△H<0,将烧瓶置于100℃的水中,则下列几项性质中不会改变的是( )
①颜色 ②平均相对分子质量 ③质量 ④压强 ⑤密度.
①颜色 ②平均相对分子质量 ③质量 ④压强 ⑤密度.
| A、①和③ | B、③和⑤ |
| C、④和⑤ | D、②和④ |
下列能用勒夏特列原理解释的是( )
①棕红色NO2加压后颜色先变深后变浅
②FeCl3溶液加热后颜色加深
③Fe(SCN)3溶液中加入固体KSCN后颜色变深
④氯水宜保存在低温、避光条件下
⑤向H2S水溶液中加入NaOH有利于S2-增多
⑥合成氨时将氨液化分离,可提高原料的利用率
⑦向AgCl悬浊液中加入KI溶液有黄色沉淀生成.
①棕红色NO2加压后颜色先变深后变浅
②FeCl3溶液加热后颜色加深
③Fe(SCN)3溶液中加入固体KSCN后颜色变深
④氯水宜保存在低温、避光条件下
⑤向H2S水溶液中加入NaOH有利于S2-增多
⑥合成氨时将氨液化分离,可提高原料的利用率
⑦向AgCl悬浊液中加入KI溶液有黄色沉淀生成.
| A、①②⑤⑥ | B、②③④⑦. |
| C、①③⑤⑦ | D、全部 |
当可逆反应2SO2+O2?2SO3达到平衡经通入18O2,再次达到平衡时,18O存在于( )
| A、SO2、O2 |
| B、SO2、SO3 |
| C、SO2、SO3、O2 |
| D、SO3、O2 |
已知化学反应速率用单位时间内某物质的浓度变化来表示,在2L容器中发生反应:3A(g)+B(g)?2C(g),若最初加入的A、B都是4mol,10s时A的物质的量为1mol,则10s内用B来表示反应速率为( )
| A、0.01 mol/(L?s) |
| B、0.2 mol/(L?s) |
| C、0.05 mol/(L?s) |
| D、0.15 mol/(L?s) |