下面是四位同学在学习“化学反应的速率和化学平衡”一章后,联系工业生产实际所发表的观点,你认为不正确的是( )
| A、使用冰箱保存食物,是利用了化学反应速率理论 |
| B、化学平衡理论是研究怎样使用有限原料多出产品 |
| C、合成氨工业的反应温度控制在500℃左右,目的是提高单位时间内的产量 |
| D、化学反应速率理论是研究怎样提高原料转化率 |
如图的原电池工作时,下列叙述正确的是( )


| A、负极反应为:Cu2++2e-=Cu |
| B、在外电路中,电流从负极流向正极 |
| C、电池总反应为:Zn+Cu2+=Zn2++Cu |
| D、盐桥中的阳离子移向负极 |
下列图示与对应的叙述不相符的是( )
A、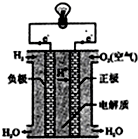 如图表示氢氧燃料电池构造示意图 |
B、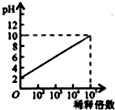 如图表示室温下pH=2的HCl溶液加水稀释倍数与pH的变化关系 |
C、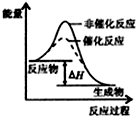 如图表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
D、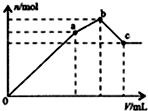 如图表示向NH4 Al(S04)2溶液中逐滴滴人Ba(OH)2溶液,生成沉淀总物质的量(n)随 着Ba(OH)2溶液体积(y)的变化 |
强酸和强碱的稀溶液的中和热可表示为:H+(aq)+OH-(aq)═H2O(l);△H=-57.3kJ/mol.
已知CH3COOH+NaOH=CH3COONa+H2O;△H=-Q1kJ/mol
H2SO4+NaOH═
Na2SO4+H2O;△H=-Q2kJ/mol
HNO3+NaOH═NaNO3+H2O;△H=-Q3kJ/mol
上述均为溶液中的反应,则Q1、Q2、Q3关系正确的是( )
已知CH3COOH+NaOH=CH3COONa+H2O;△H=-Q1kJ/mol
| 1 |
| 2 |
| 1 |
| 2 |
HNO3+NaOH═NaNO3+H2O;△H=-Q3kJ/mol
上述均为溶液中的反应,则Q1、Q2、Q3关系正确的是( )
| A、Q1=Q2=Q3 |
| B、Q2>Q3>Q1 |
| C、Q1>Q2>Q3 |
| D、Q1<Q2═Q3 |
已知滤渣2的主要成分是Fe(OH)3和Al(OH)3,由滤渣2制取Al2(SO4)3?18H2O,该探究小组设计了如下实验方案:

下列关于此方案的说法,错误的是( )

下列关于此方案的说法,错误的是( )
| A、加入NaOH溶液后过滤,滤渣为Fe(OH)3 |
| B、也可以先加硫酸,再加NaOH溶液后蒸发、冷却、结晶、过滤 |
| C、加硫酸后,溶液中的盐除含有硫酸铝外,还有硫酸钠 |
| D、如果滤渣2中含1molAl(OH)3,则至少需要1molNaOH才能使Al(OH)3完全溶解 |
化学与生活密切相关,下列说法错误的是( )
| A、含有重金属的电器废品不能随意丢弃,要分类回收并利用 |
| B、食品中都必须添加大量的化学防腐剂,使食品保质期更长久, |
| C、采用加热消毒的目的是使蛋白质变性而杀灭细菌消毒 |
| D、使用乙醇作为汽油的代用品,可以减少汽车尾气中有害气体排放 |
下列金属防腐的措施中,使用外加电流的阴极保护法的是( )
| A、水中的钢闸门连接电源的负极 |
| B、金属护拦表面涂漆 |
| C、枪炮表面涂上一层油 |
| D、地下钢管连接镁块 |
写出下列反应的化学方程式
(1)Na2O2与CO2反应
(2)将氯气与通入冷的消石灰中反应制漂白粉
(3)向较浓的Na2SiO3溶液中滴加适量盐酸制得硅酸胶体
(4)碳酸氢钠溶液中滴加入NaOH溶液 .
(1)Na2O2与CO2反应
(2)将氯气与通入冷的消石灰中反应制漂白粉
(3)向较浓的Na2SiO3溶液中滴加适量盐酸制得硅酸胶体
(4)碳酸氢钠溶液中滴加入NaOH溶液
下列化合物中,只能在溶液中才能导电的电解质是( )
| A、NaCl |
| B、H2SO4 |
| C、NH3 |
| D、CaO |
 氢氧燃料电池是符合绿色化学理念的新型发电装置.图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置.图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答: