题目内容
强酸和强碱的稀溶液的中和热可表示为:H+(aq)+OH-(aq)═H2O(l);△H=-57.3kJ/mol.
已知CH3COOH+NaOH=CH3COONa+H2O;△H=-Q1kJ/mol
H2SO4+NaOH═
Na2SO4+H2O;△H=-Q2kJ/mol
HNO3+NaOH═NaNO3+H2O;△H=-Q3kJ/mol
上述均为溶液中的反应,则Q1、Q2、Q3关系正确的是( )
已知CH3COOH+NaOH=CH3COONa+H2O;△H=-Q1kJ/mol
| 1 |
| 2 |
| 1 |
| 2 |
HNO3+NaOH═NaNO3+H2O;△H=-Q3kJ/mol
上述均为溶液中的反应,则Q1、Q2、Q3关系正确的是( )
| A、Q1=Q2=Q3 |
| B、Q2>Q3>Q1 |
| C、Q1>Q2>Q3 |
| D、Q1<Q2═Q3 |
考点:反应热的大小比较
专题:化学反应中的能量变化
分析:稀的强酸与强碱生成1molH2O放出的热量为中和热,注意弱电解质的电离吸热来解答.
解答:
解:强酸与强碱的稀溶液发生中和反应的热效应:H+(aq)十OH-(aq)=H2O△H=-57.3kJ/mol,
醋酸的电离吸热,放出的热量Q1小于57.3kJ,而稀硫酸、稀硝酸为稀的强酸,中和热相同,所以Q2=Q3>Q1,
故选D.
醋酸的电离吸热,放出的热量Q1小于57.3kJ,而稀硫酸、稀硝酸为稀的强酸,中和热相同,所以Q2=Q3>Q1,
故选D.
点评:本题考查中和热,明确中和热的概念及弱电解质的电离吸热即可解答,题目难度不大.

练习册系列答案
 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
25℃时,已知弱酸的电离常数:Ki(CH3COOH)=1.8×10-5;Ki1(H2CO3)=4.4×10-7;Ki2(H2CO3)=4.7×10-11;Ki(HClO)=4.0×10-8.则下列说法正确的是( )
| A、物质的量浓度相等的溶液pH关系:pH(NaClO)>pH(Na2CO3)>pH(CH3COONa) |
| B、向NaClO溶液中通少量CO2:CO2+NaClO+H2O→NaHCO3+HClO |
| C、a mol/L HClO与b mol/L NaOH溶液等体积混合后所得溶液中c(Na+)>c(ClO-),则a一定小于b |
| D、向氯水中加入NaHCO3固体,可以增大氯水中次氯酸的浓度 |
写出下列反应的化学方程式
(1)Na2O2与CO2反应
(2)将氯气与通入冷的消石灰中反应制漂白粉
(3)向较浓的Na2SiO3溶液中滴加适量盐酸制得硅酸胶体
(4)碳酸氢钠溶液中滴加入NaOH溶液 .
(1)Na2O2与CO2反应
(2)将氯气与通入冷的消石灰中反应制漂白粉
(3)向较浓的Na2SiO3溶液中滴加适量盐酸制得硅酸胶体
(4)碳酸氢钠溶液中滴加入NaOH溶液
能将化学能转化为电能的装置(烧杯中溶液均为稀硫酸)是( )
A、 |
B、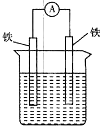 |
C、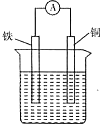 |
D、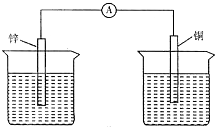 |
下列有关活化能的说法正确的是( )
| A、Ag+和Cl-在水溶液中混合,其反应的活化能接近于零 |
| B、活化能的大小对化学反应前后的能量变化能产生影响 |
| C、加催化剂能降低正反应的活化能,但不降低逆反应的活化能 |
| D、温度降低,反应速率减慢,其原因是降低了反应的活化能 |
下列有关的离子方程式书写正确的是( )
| A、氢氧化钡溶液和稀硫酸反应:Ba2++SO42-=BaSO4↓ |
| B、浓盐酸与铁屑反应:2Fe+6H+=2Fe3++3H2↑ |
| C、SO2通入溴水中:SO2+Br2+2H2O=SO42-+2Br-+4H+ |
| D、钠放于水中:Na+2H2O=Na++2OH-+H2↑ |
 如图在下衬白纸的玻璃片中央放置适量的KMnO4颗粒,在周围分别滴加一滴KBr溶液,品红溶液,含有酚酞的澄清石灰水,FeC12溶液,然后在KMnO4晶体上滴加适量的浓盐酸,迅速盖好表面皿.提示:实验室中所用的少量氯气可以用下述原理制取:
如图在下衬白纸的玻璃片中央放置适量的KMnO4颗粒,在周围分别滴加一滴KBr溶液,品红溶液,含有酚酞的澄清石灰水,FeC12溶液,然后在KMnO4晶体上滴加适量的浓盐酸,迅速盖好表面皿.提示:实验室中所用的少量氯气可以用下述原理制取: