题目内容
下列金属防腐的措施中,使用外加电流的阴极保护法的是( )
| A、水中的钢闸门连接电源的负极 |
| B、金属护拦表面涂漆 |
| C、枪炮表面涂上一层油 |
| D、地下钢管连接镁块 |
考点:金属的电化学腐蚀与防护
专题:
分析:金属防腐的措施中,使用外加电流的阴极保护法,说明被保护的金属连接未加电源的负极,该方法使用电化学中的电解池原理,据此分析解答.
解答:
解:金属防腐的措施中,使用外加电流的阴极保护法,说明被保护的金属连接未加电源的负极,该方法使用电化学中的电解池原理,
A.水中的钢闸门连接电源的负极,符合题意,故A正确;
B.金属护栏表面涂漆,属于物理方法,不符合题意,故B错误;
C.枪炮表面涂上一层油属于物理方法,不符合题意,故C错误;
D.地下钢管连接镁属于电化学方法,但属于原电池原理,故D错误;
故选A.
A.水中的钢闸门连接电源的负极,符合题意,故A正确;
B.金属护栏表面涂漆,属于物理方法,不符合题意,故B错误;
C.枪炮表面涂上一层油属于物理方法,不符合题意,故C错误;
D.地下钢管连接镁属于电化学方法,但属于原电池原理,故D错误;
故选A.
点评:本题考查金属的电化学腐蚀与防护,明确原电池和电解池原理即可解答,利用电化学原理保护金属意义重大.

练习册系列答案
相关题目
温度为T℃时,向2.0L恒容密闭容器中充入1.0molPCl5,反应PCl5(g)?PCl3(g)+Cl2(g)经一段时间后达到平衡.反应过程中测定的部分数据见下表:下列说法正确的是( )
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A、反应在前50 s的平均速率为v(PCl3)=0.0032mol?L-1?s-1 |
| B、保持其他条件不变,升高温度,平衡时,c(PCl3)=0.11mol?L-1,则反应的△H<0 |
| C、相同温度下,起始时向容器中充入1.0molPCl5、0.20molPCl3和0.20molCl2,达到平衡前v(正)>v(逆) |
| D、相同温度下,起始时向容器中充入2.0molPCl5、2.0molCl2,达到平衡时,PCl5的转化率大于20% |
下列图示与对应的叙述不相符的是( )
A、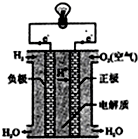 如图表示氢氧燃料电池构造示意图 |
B、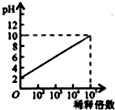 如图表示室温下pH=2的HCl溶液加水稀释倍数与pH的变化关系 |
C、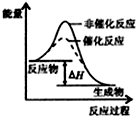 如图表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
D、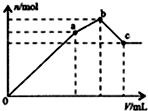 如图表示向NH4 Al(S04)2溶液中逐滴滴人Ba(OH)2溶液,生成沉淀总物质的量(n)随 着Ba(OH)2溶液体积(y)的变化 |
对于硫酸工业中SO2的催化氧化反应:2SO2+O2
2SO3,下列说法错误的是( )
| 催化剂 |
| 加热 |
| A、使用催化剂是为了加快反应速率 |
| B、增大O2浓度可以使SO2转化率达到100% |
| C、加压可以增大反应速率 |
| D、增大O2浓度可以增大反应速率 |
金属钠着火时,可以灭火的物质或器材是( )
| A、水 | B、砂子 |
| C、泡沫灭火器 | D、干粉灭火器 |
下列叙述正确的是( )
| A、1 mol H2O的质量为18g/mol |
| B、CH4的摩尔质量为16g |
| C、阿伏伽德罗常数个SO2分子的质量为64g |
| D、标准状况下,1 mol任何物质体积均为22.4L |