还原沉淀法是处理含铬(含Cr2072-和CrO42-)工业废水的常用方法,过程如下:CrO
Cr2O
Cr 3+
Cr(OH)3↓已知转化过程中的反应为:2CrO
(aq)+2H+ (aq)?Cr2O
(aq)+H2O(l).转化后所得溶液中铬元素的含量为28.6g/L,CrO42-有
转化为Cr2072-,下列说法不正确的是( )
2- 4 |
| H+ |
| 转换 |
2- 7 |
| Fe2+ |
| 还原 |
| OH- |
| 沉淀 |
2- 4 |
2- 7 |
| 10 |
| 11 |
| A、溶液颜色保持不变,说明上述可逆反应达到平衡状态 |
| B、若用绿矾(FeS04?7H20)(M=278)作还原剂,处理1 L废水,至少需要917.4 g |
| C、常温下转化反应的平衡常数K=1×1014,则转化后所得溶液的pH=6 |
| D、常温下Ksp[Cr(OH)3]=1×10-32,要使处理后废水中的c(Cr3+)降至1×10-5mol/L,应调溶液的pH=5 |
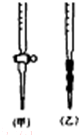
如图为周期表前四周期的一部分,关于X、Y、Z、M的说法正确的是( )
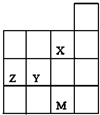

| A、Y、Z的最高价氧化物的水化物酸性为Y<Z |
| B、M的最外层电子数比Z大10 |
| C、X、M的气态氢化物的稳定性M>X |
| D、X、Y形成简单离子的最外层电子均满足8e-稳定结构 |
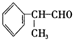 是一种重要的化工原料,其合成路线如下:
是一种重要的化工原料,其合成路线如下: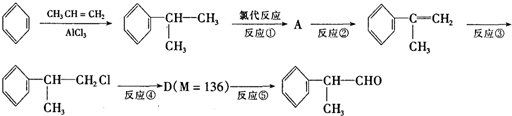
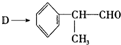 反应的化学方程式为
反应的化学方程式为
 )和多巴胺的结构相似,它的核磁共振氢谱中可以发现有
)和多巴胺的结构相似,它的核磁共振氢谱中可以发现有

 制成,合成路线如下:
制成,合成路线如下:

 )(用反应流程图表示).
)(用反应流程图表示).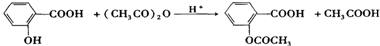
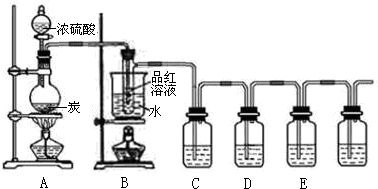
 阅读下列实验内容,根据题目要求回答问题.
阅读下列实验内容,根据题目要求回答问题.