题目内容
某同学设计如下实验验证炭与浓硫酸的反应产物及产物的某些性质.
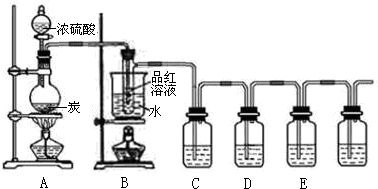
(1)装置A中盛放浓硫酸的仪器名称是 .
(2)若要证明有水生成,需要在A、B之间加装盛有 的干燥管.
(3)利用装置B可以完成的实验是 .
(4)若在E中盛装澄清石灰水,C中盛装酸性高锰酸钾溶液,则D中的试剂是 ,其作用是 ;写出C中关于高锰酸钾发生反应的离子方程式 .

(1)装置A中盛放浓硫酸的仪器名称是
(2)若要证明有水生成,需要在A、B之间加装盛有
(3)利用装置B可以完成的实验是
(4)若在E中盛装澄清石灰水,C中盛装酸性高锰酸钾溶液,则D中的试剂是
考点:浓硫酸的性质实验
专题:实验题
分析:(1)盛放浓硫酸的仪器是分液漏斗;
(2)水能使无水硫酸铜变蓝色,所以可以用无水硫酸铜检验水蒸气;
(3)二氧化硫能和有色物质反应生成无色物质而具有漂白性,但二氧化硫的漂白性不稳定,受热易恢复原色;
(4)二氧化硫具有还原性,能被强氧化剂氧化,二氧化硫、二氧化碳都能使澄清石灰水变浑浊,要用澄清石灰水检验二氧化碳,需要先除去二氧化硫的干扰,所以D中试剂是品红溶液或酸性高锰酸钾溶液;二氧化硫和高锰酸钾反应生成锰离子、硫酸根离子和氢离子.
(2)水能使无水硫酸铜变蓝色,所以可以用无水硫酸铜检验水蒸气;
(3)二氧化硫能和有色物质反应生成无色物质而具有漂白性,但二氧化硫的漂白性不稳定,受热易恢复原色;
(4)二氧化硫具有还原性,能被强氧化剂氧化,二氧化硫、二氧化碳都能使澄清石灰水变浑浊,要用澄清石灰水检验二氧化碳,需要先除去二氧化硫的干扰,所以D中试剂是品红溶液或酸性高锰酸钾溶液;二氧化硫和高锰酸钾反应生成锰离子、硫酸根离子和氢离子.
解答:
解:(1)盛放浓硫酸的仪器是分液漏斗,所以该仪器名称是分液漏斗,故答案为:分液漏斗;
(2)水能使无水硫酸铜变蓝色,所以可以用无水硫酸铜检验水蒸气,则若要证明有水生成,需要在A、B之间加装盛有无水硫酸铜的干燥管,故答案为:无水硫酸铜;
(3)二氧化硫能和有色物质反应生成无色物质而具有漂白性,但二氧化硫的漂白性不稳定,受热易恢复原色,所以利用装置B可以完成的实验是:探究SO2与品红反应的可逆性(写“加热可以使品红恢复红色”或相近意思也可),故答案为:探究SO2与品红反应的可逆性(写“加热可以使品红恢复红色”或相近意思也可);
(4)二氧化硫具有还原性,能被强氧化剂氧化,二氧化硫、二氧化碳都能使澄清石灰水变浑浊,要用澄清石灰水检验二氧化碳,需要先除去二氧化硫的干扰,所以D中试剂是品红溶液或酸性高锰酸钾溶液,其目的是确认二氧化硫是否除尽;二氧化硫和高锰酸钾反应生成锰离子、硫酸根离子和氢离子,离子方程式为2MnO4-+5SO2+2H2O=2Mn2++5SO42-+4H+,故答案为:品红溶液(酸性高锰酸钾溶液);检验二氧化硫已经除尽;2MnO4-+5SO2+2H2O=2Mn2++5SO42-+4H+.
(2)水能使无水硫酸铜变蓝色,所以可以用无水硫酸铜检验水蒸气,则若要证明有水生成,需要在A、B之间加装盛有无水硫酸铜的干燥管,故答案为:无水硫酸铜;
(3)二氧化硫能和有色物质反应生成无色物质而具有漂白性,但二氧化硫的漂白性不稳定,受热易恢复原色,所以利用装置B可以完成的实验是:探究SO2与品红反应的可逆性(写“加热可以使品红恢复红色”或相近意思也可),故答案为:探究SO2与品红反应的可逆性(写“加热可以使品红恢复红色”或相近意思也可);
(4)二氧化硫具有还原性,能被强氧化剂氧化,二氧化硫、二氧化碳都能使澄清石灰水变浑浊,要用澄清石灰水检验二氧化碳,需要先除去二氧化硫的干扰,所以D中试剂是品红溶液或酸性高锰酸钾溶液,其目的是确认二氧化硫是否除尽;二氧化硫和高锰酸钾反应生成锰离子、硫酸根离子和氢离子,离子方程式为2MnO4-+5SO2+2H2O=2Mn2++5SO42-+4H+,故答案为:品红溶液(酸性高锰酸钾溶液);检验二氧化硫已经除尽;2MnO4-+5SO2+2H2O=2Mn2++5SO42-+4H+.
点评:本题考查浓硫酸性质实验,侧重考查实验操作、分析能力,明确物质的性质是解本题关键,注意二氧化硫和二氧化碳都能使澄清石灰水变浑浊,注意二氧化硫不能使酸碱指示剂褪色,为易错点.

练习册系列答案
相关题目
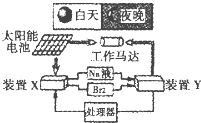 如图是设计的一种航天器能量储存系统原理示意图.它是利用太阳能和物质间的物质变化和能量转换实现循环使用.下列说法正确的是( )
如图是设计的一种航天器能量储存系统原理示意图.它是利用太阳能和物质间的物质变化和能量转换实现循环使用.下列说法正确的是( )| A、二氧化硅是太阳能电池的光电转换材料 |
| B、装置X中阳极反应式:Br2+2e-2Br- |
| C、装置Y中正极反应式为:Br2+2e-2Br- |
| D、有了这套装置后就不用考虑节能减排了 |
如表为元素周期表短周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )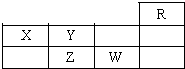

| A、常压下五种元素的单质中W单质的沸点最高 |
| B、Z的氢化物比Y的氢化物稳定 |
| C、W元素最高价氧化物的水化物酸性比Z元素的强 |
| D、Z、W的阴离子电子层结构与R原子的相同 |
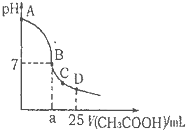 在25mL 0.1mol?L-1 NaOH溶液中逐滴加入0.2mol?L-1 CH3COOH溶液,溶液pH变化曲线如图所示,下列有关离子浓度的比较正确的是( )
在25mL 0.1mol?L-1 NaOH溶液中逐滴加入0.2mol?L-1 CH3COOH溶液,溶液pH变化曲线如图所示,下列有关离子浓度的比较正确的是( )| A、在A、B间任一点(不含A、B点),溶液中可能有c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| B、在C点,c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
| C、在B点,a>12.5,且有c(Na+)=c(CH3COO-)>c(OH-)>c(H+) |
| D、在D点,c(CH3COO-)+c(CH3COOH)=c(Na+) |
下列关于电解饱和食盐水所用的离子交换膜、电解槽的叙述错误的是( )
| A、精制饱和食盐水进入阳极室 |
| B、纯水(加少量NaOH)进入阴极室 |
| C、阳极产物为氢氧化钠和氢气 |
| D、阳极的电极反应:Cl2+2e-═2Cl- |
化学与生活密切相关,下列有关说法正确的是( )
| A、加热能杀死H1N1流感病毒是因为病毒蛋白质受热变性 |
| B、不锈钢是利用了牺牲阳极的阴极保护法来达到防止腐蚀的目的 |
| C、明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理相同 |
| D、加碘食盐中主要添加的是碘化钾 |
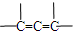 ”结构的有机物不能稳定存在.请结合(1)、(2)有关信息,分析如下转化关系,回答问题:
”结构的有机物不能稳定存在.请结合(1)、(2)有关信息,分析如下转化关系,回答问题: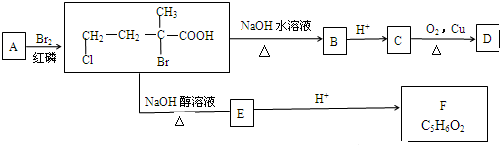


 ,写出由G生成I的化学反应方程式
,写出由G生成I的化学反应方程式