设NA为阿佛加德罗常数的数值,下列说法正确的是( )
| A、常温常压下,8gO2含有4NA个电子 |
| B、1L1mol/L的K2SO4中有NA个K+ |
| C、标准状况下,22.4L盐酸含有NA个HCl分子 |
| D、1molNa被完全氧化生成Na2O2,失去个NA电子 |
 下列是某兴趣小组根据课本实验设计的一个能说明碳酸钠与碳酸氢钠热稳定性的套管实验.请观察如图的实验装置、分析实验原理,下列说法错误的是( )
下列是某兴趣小组根据课本实验设计的一个能说明碳酸钠与碳酸氢钠热稳定性的套管实验.请观察如图的实验装置、分析实验原理,下列说法错误的是( )| A、甲为纯碱,乙为小苏打 |
| B、要证明碳酸氢钠受热能产生水,可在小试管内塞上沾有无水硫酸铜粉末的棉花球 |
| C、整个实验过程中可以看到丙烧杯的澄清石灰水没变浑浊 |
| D、同质量的甲和乙完全反应消耗的同浓度的盐酸体积:甲>乙 |
下列物质之间的转化都一步能实现的是( )
| A、Si→SiO2→H2SiO3→Na2SiO3 |
| B、Al→Al2O3→Al(OH)3→NaAlO2 |
| C、Na→NaOH→Na2CO3→NaHCO3 |
| D、Cu→CuO→Cu(OH)2→CuSO4 |

 某同学设计如图所示装置(部分夹持装置已略去),该装置可以用来进行多项实验研究.
某同学设计如图所示装置(部分夹持装置已略去),该装置可以用来进行多项实验研究.
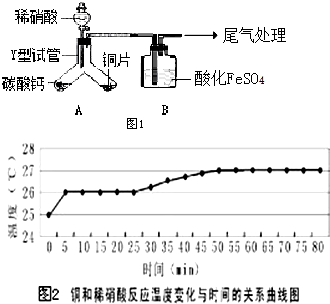 为探究铜与稀硝酸反应的产物及影响反应速率的主要因素,进行如下实验.
为探究铜与稀硝酸反应的产物及影响反应速率的主要因素,进行如下实验.