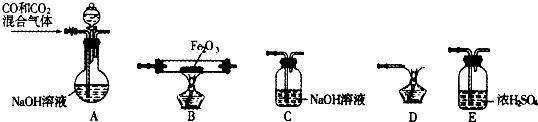
��Ŀ����
MnO2����Ҫ�����ϣ�ij�о���ѧϰС������˽���MnO2�����н϶��MnO��MnCO3����Ʒת��Ϊ��MnO2ʵ�飬����������

����֪��������ǿ��˳��ClO3-��MnO2��Fe2+��
��1��������������ڸ����·������ȷ�Ӧ����ط�Ӧ�Ļ�ѧ����ʽΪ�� ��
��2���ڢڲ���Ӧ���ӷ���ʽΪ�� ��
��3���ڢ۲������������������������̨������Ȧ������������ �� ���ڢ۲������õ��Ĺ����г���NaClO3��NaOH����һ������ ��д��ѧʽ����
��4��MnO2�Ǽ���п�̵�ص��������ϣ������п�̵�طŵ�ʱ�������ĵ缫��Ӧʽ�� ��
��5������MnO2��Ʒ�е�����Ϊ28.2g���ڢٲ���Ӧ�����˵õ�17.4g MnO2�����ռ���448mL CO2����״���£������ڵڢڲ���Ӧ��������Ҫ mol NaClO3���ܽ�Mn2+��ȫת��ΪMnO2��

����֪��������ǿ��˳��ClO3-��MnO2��Fe2+��
��1��������������ڸ����·������ȷ�Ӧ����ط�Ӧ�Ļ�ѧ����ʽΪ��
��2���ڢڲ���Ӧ���ӷ���ʽΪ��
��3���ڢ۲������������������������̨������Ȧ������������
��4��MnO2�Ǽ���п�̵�ص��������ϣ������п�̵�طŵ�ʱ�������ĵ缫��Ӧʽ��
��5������MnO2��Ʒ�е�����Ϊ28.2g���ڢٲ���Ӧ�����˵õ�17.4g MnO2�����ռ���448mL CO2����״���£������ڵڢڲ���Ӧ��������Ҫ
���㣺���ʷ�����ᴿ�ķ����ͻ��������ۺ�Ӧ��
ר�⣺ʵ�������
��������MnO2�����н϶��MnO��MnCO3����Ʒ�м��������ϡ���ᣬ����MnO2���������ᣬ����Ʒ�е�MnO��MnCO3�ֱ�����ᷴӦ���ɿ����Ե�MnSO4�����˵���Һ��Ϊ��������Һ������NaClO3������ӦΪ��5Mn2++2ClO3-+4H2O=5MnO2+Cl2��+8H+���ٹ��˵õ���Һ��Ͷ������̹��壬���������ȵ��������Ʒ�Ӧ���������Ʒ���ʽΪ��3Cl2+6NaOH=NaClO3+NaCl+3H2O��
��1��������������ڸ����·������ȷ�Ӧ�������������̣��ݴ�д����Ӧ�ķ���ʽ��
��2�����ݵ�ʧ�����غ�������غ��д�����ӷ���ʽ��
��3���������������������̨������Ȧ�����ƾ��ơ�������������Cl2ͨ���ȵ�NaOH��Һ����NaClO3��NaCl���ɣ�
��4������ԭ��ع���ԭ���ж�����������ԭ��Ӧ��Ȼ������ܷ�Ӧд�������ĵ缫��Ӧʽ��
��5�����������غ�ͻ�ѧ����ʽ���㣬CO2�����ʵ���Ϊ0.02mol����MnCO3�����ʵ���Ϊ0.02mol������Ϊ��115g/mol��0.0��2mol=2.3������MnO������Ϊ28.2g-17.4g-2.3g=8.5g�������ʵ���Ϊ
=0.12mol�������ϡ���ᷴӦʱ������MnSO4�����ʵ���Ϊ0.14mol�����ݷ���ʽ5MnSO4+2NaClO3+4H2O=5MnO2+Cl2��+Na2SO4+4H2SO4���ɼ������ҪNaClO3�����ʵ���Ϊ0.056mol��
��1��������������ڸ����·������ȷ�Ӧ�������������̣��ݴ�д����Ӧ�ķ���ʽ��
��2�����ݵ�ʧ�����غ�������غ��д�����ӷ���ʽ��
��3���������������������̨������Ȧ�����ƾ��ơ�������������Cl2ͨ���ȵ�NaOH��Һ����NaClO3��NaCl���ɣ�
��4������ԭ��ع���ԭ���ж�����������ԭ��Ӧ��Ȼ������ܷ�Ӧд�������ĵ缫��Ӧʽ��
��5�����������غ�ͻ�ѧ����ʽ���㣬CO2�����ʵ���Ϊ0.02mol����MnCO3�����ʵ���Ϊ0.02mol������Ϊ��115g/mol��0.0��2mol=2.3������MnO������Ϊ28.2g-17.4g-2.3g=8.5g�������ʵ���Ϊ
| 8.5g |
| 71g/mol |
���
�⣺��MnO2�����н϶��MnO��MnCO3����Ʒ�м��������ϡ���ᣬ����MnO2���������ᣬ����Ʒ�е�MnO��MnCO3�ֱ�����ᷴӦ���ɿ����Ե�MnSO4�����˵���Һ��Ϊ��������Һ������NaClO3������ӦΪ��5Mn2++2ClO3-+4H2O=5MnO2+Cl2��+8H+���ٹ��˵õ���Һ��Ͷ������̹��壬���������ȵ��������Ʒ�Ӧ���������Ʒ���ʽΪ��3Cl2+6NaOH=NaClO3+NaCl+3H2O��
��1��������������ڸ����·������ȷ�Ӧ����Ӧ�Ļ�ѧ����ʽΪ��3MnO2+4Al
2Al2O3+3Mn��
�ʴ�Ϊ��3MnO2+4Al
2Al2O3+3Mn��
��2��MnSO4Ҫת��ΪMnO2����ʧȥ���ӣ�����Ҫ����NaClO3�������������ݵ�ʧ�����غ������ƽ�����Է�Ӧ�Ļ�ѧ����ʽ�ǣ�5MnSO4+2NaClO3+4H2O=5MnO2+Cl2��+Na2SO4+4H2SO4����˷�Ӧ�����ӷ���ʽ�ǣ�5Mn2++2ClO3-+4H2O=5MnO2+Cl2��+8H+��
�ʴ�Ϊ��5Mn2++2ClO3-+4H2O=5MnO2+Cl2��+8H+��
��3���ڢ������������������������������̨������Ȧ�����ƾ��ơ�������������Cl2ͨ���ȵ�NaOH��Һ��һ������������ԭ��Ӧ������������������������ԭ����NaClO3��������������һ���л�ԭ����NaCl��
�ʴ�Ϊ���ƾ��ƣ�������NaCl��
��4��ԭ����и���ʧȥ���ӣ������õ����ӣ���˼���п�̵�طŵ�ʱ�������Ƕ������̵õ����ӣ���缫��ӦʽΪ��MnO2+H2O+e-=MnO��OH��+OH-��
�ʴ�Ϊ��MnO2+H2O+e-�TMnOOH+OH-��
��5�����ɵ�CO2�����ʵ���Ϊ��
=0.02mol����MnCO3�����ʵ���Ϊ0.02mol��̼���̵�����Ϊ��115g/mol��0.0��2mol=2.3��
�������MnO������Ϊ��28.2g-17.4g-2.3g=8.5g��MnO�����ʵ���Ϊ��
=0.12mol��
�����ϡ���ᷴӦʱ������MnSO4�����ʵ���Ϊ��0.02mol+0.12mol=0.14mol��
���ݷ���ʽ5MnSO4+2NaClO3+4H2O=5MnO2+Cl2��+Na2SO4+4H2SO4���ɼ������ҪNaClO3�����ʵ���Ϊ��0.14mol��
=0.056mol��
�ʴ�Ϊ��0.056��
��1��������������ڸ����·������ȷ�Ӧ����Ӧ�Ļ�ѧ����ʽΪ��3MnO2+4Al
| ||
�ʴ�Ϊ��3MnO2+4Al
| ||
��2��MnSO4Ҫת��ΪMnO2����ʧȥ���ӣ�����Ҫ����NaClO3�������������ݵ�ʧ�����غ������ƽ�����Է�Ӧ�Ļ�ѧ����ʽ�ǣ�5MnSO4+2NaClO3+4H2O=5MnO2+Cl2��+Na2SO4+4H2SO4����˷�Ӧ�����ӷ���ʽ�ǣ�5Mn2++2ClO3-+4H2O=5MnO2+Cl2��+8H+��
�ʴ�Ϊ��5Mn2++2ClO3-+4H2O=5MnO2+Cl2��+8H+��
��3���ڢ������������������������������̨������Ȧ�����ƾ��ơ�������������Cl2ͨ���ȵ�NaOH��Һ��һ������������ԭ��Ӧ������������������������ԭ����NaClO3��������������һ���л�ԭ����NaCl��
�ʴ�Ϊ���ƾ��ƣ�������NaCl��
��4��ԭ����и���ʧȥ���ӣ������õ����ӣ���˼���п�̵�طŵ�ʱ�������Ƕ������̵õ����ӣ���缫��ӦʽΪ��MnO2+H2O+e-=MnO��OH��+OH-��
�ʴ�Ϊ��MnO2+H2O+e-�TMnOOH+OH-��
��5�����ɵ�CO2�����ʵ���Ϊ��
| 0.448L |
| 22.4L/mol |
�������MnO������Ϊ��28.2g-17.4g-2.3g=8.5g��MnO�����ʵ���Ϊ��
| 8.5g |
| 71g/mol |
�����ϡ���ᷴӦʱ������MnSO4�����ʵ���Ϊ��0.02mol+0.12mol=0.14mol��
���ݷ���ʽ5MnSO4+2NaClO3+4H2O=5MnO2+Cl2��+Na2SO4+4H2SO4���ɼ������ҪNaClO3�����ʵ���Ϊ��0.14mol��
| 2 |
| 5 |
�ʴ�Ϊ��0.056��
���������⿼�����ʵķ������ᴿ�������ۺ�Ӧ�ã�Ϊ��Ƶ���㣬��Ŀ�Ѷ��еȣ����������з����Ļ�ѧ��Ӧ���������뷽��Ϊ���Ĺؼ���ע�����ջ�ѧʵ���������������������ط����������ƶ������Ŀ��飮

��ϰ��ϵ�д�
�����Ŀ
����˵����ȷ���ǣ�������
| A�����ᡢ��������ƺ���ʯ�ҷֱ������ᡢ��κ������� |
| B��̼���ơ������������Ȼ�李��������ƶ��������ӻ����� |
| C��ʯ̿�ᡢʯ�͡��ռ�ֱ������ᡢ��֬���� |
| D�����ǡ�����غ����ᱵ�ֱ����ڷǵ���ʡ�ǿ����ʺ�������� |
ʵ������ȡ��������ķ�Ӧ�������ӷ�Ӧ���ǣ�������
��H2 ��O2 ��CO2��
��H2 ��O2 ��CO2��
| A���٢ڢ� | B���٢� | C���٢� | D���ڢ� |
ij100mL������У�HNO3���ʵ���Ũ��Ϊ0.4mol/L��H2SO4�ʵ���Ũ��Ϊ0.2mol/�������м���2.56��Cu�ۣ�����ַ�Ӧ����Һ�е�Cu2+�����ʵ���Ũ���ǣ�������
| A��0.15mol/L |
| B��0.3mol/L |
| C��0.225mol/L |
| D�������� |
��������Һ�У���������һ���ܹ�����������ǣ�������
| A����ˮ�����c��H+��=1��10-14mol?L-1����Һ�У�Ca2+��K+��Cl-��HCO3- |
| B����pH=1����ɫ��Һ��Fe2+��Mg2+��NO3-��Cl- |
| C�����д���Al3+����Һ��Na+��C1-��NO3-��OH- |
| D��������OH-����Һ�У�CO32-��Cl-��F-��K+ |
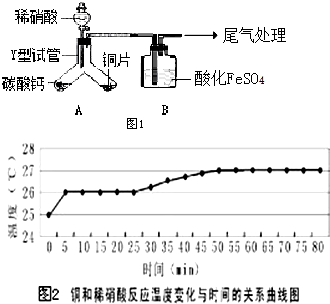 Ϊ̽��ͭ��ϡ���ᷴӦ�IJ��PӰ�췴Ӧ���ʵ���Ҫ���أ���������ʵ�飮
Ϊ̽��ͭ��ϡ���ᷴӦ�IJ��PӰ�췴Ӧ���ʵ���Ҫ���أ���������ʵ�飮