铅蓄电池的两极分别为Pb、PbO2,电解质溶液为H2SO4,工作时的反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O,下列结论正确的是( )
| A、Pb 为正极被氧化 |
| B、溶液的pH不断减小 |
| C、放电时负极反应式是PbO2+4H++SO42-+2e-=PbSO4+2H2O |
| D、溶液pH不断增大 |
水的离子积常数(KW)、电离常数(Ka、Kb)、溶度积常数(Ksp)等都是表示、判断物质性质的重要常数,下列关于这些常数的说法中,正确的是( )
| A、稀溶液中水的离子积常数的大小与温度、浓度有关 |
| B、Ka(HCN)<Ka(CH3COOH)说明相同物质的量浓度时,氢氰酸的酸性比醋酸强 |
| C、向氯化钡溶液中滴入同浓度的碳酸钠和硫酸钠溶液,先产生BaSO4沉淀,则Ksp(BaSO4)>Ksp(BaCO3) |
| D、当温度升高时,弱酸电离常数(Ka)变大,弱碱电离常数(Kb)变大 |
由水电离出的c(H+)=10-13mol/L的溶液中,一定能大量共存的离子 ( )
| A、K+、Na+、HCO3-、Cl- |
| B、K+、Br-、AlO2-、Cl- |
| C、SO42-、Na+、NO3-、Cl- |
| D、SO42-、NH4+、Al3+、Cl- |
下列关于甲、乙、丙、丁四个图象的说法中,正确的是( )
A、 是等质量的两份锌粉a、b分别加到过量的稀硫酸中,同时向a中加入少量CH3COONa溶液,产生H2的体积V(L)与时间t(min)的关系图 |
B、 足量CO2不断通入含KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀与通入CO2的体积的关系图 |
C、 由图可知,双氧水在有催化剂存在时的热化学方程式为:2H2O2(l)=2H2O(l)+O2(g)△H=-2(Ea2′-Ea2) kJ?mol-1 |
D、 装置图能实现铁上镀锌 |
某温度下,在一体积恒定的密闭容器内发生反应:A(s)+2B(g)?C(g)+D(g),当下列物理量不再变化时,不能表明反应已达平衡的是( )
| A、混合气体的压强 |
| B、混合气体的平均摩尔质量 |
| C、混合气体的密度 |
| D、混合气体的质量 |
在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表下列说法错误的是:( )
| 物质 | X | Y | Z |
| 初始浓度/mol?L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度mol?L-1 | 0.05 | 0.05 | 0.1 |
| A、反应达到平衡时,X的转化率为50% |
| B、反应可表示为X+3Y?2Z |
| C、增大压强使平衡向生成Z的方向移动 |
| D、加入催化剂可以使平衡向右移动 |



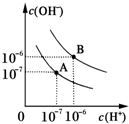 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示: