题目内容
某温度下,在一体积恒定的密闭容器内发生反应:A(s)+2B(g)?C(g)+D(g),当下列物理量不再变化时,不能表明反应已达平衡的是( )
| A、混合气体的压强 |
| B、混合气体的平均摩尔质量 |
| C、混合气体的密度 |
| D、混合气体的质量 |
考点:化学平衡状态的判断
专题:化学平衡专题
分析:该反应是一个反应前后气体体积不变的可逆反应,只有反应前后改变的物理量不变时,该反应就达到平衡状态,据此分析解答.
解答:
解:A.该反应是一个反应前后气体体积不变的可逆反应,所以无论是否达到平衡状态,压强始终不变,所以不能根据混合气体压强判断平衡状态,故A选;
B.该反应前后气体质量改变、物质的量不变,所以其平均摩尔质量改变,当混合气体的平均摩尔质量不变时该反应达到平衡状态,故B不选;
C.该反应前后气体质量改变、容器的体积不变,所以其密度改变,当混合气体的密度不变时该反应达到平衡状态,故C不选;
D.根据质量守恒知,反应物有固体、生成物没有固体,所以反应前后气体质量改变,当混合气体的质量不变时该反应达到平衡状态,故D不选;
故选A.
B.该反应前后气体质量改变、物质的量不变,所以其平均摩尔质量改变,当混合气体的平均摩尔质量不变时该反应达到平衡状态,故B不选;
C.该反应前后气体质量改变、容器的体积不变,所以其密度改变,当混合气体的密度不变时该反应达到平衡状态,故C不选;
D.根据质量守恒知,反应物有固体、生成物没有固体,所以反应前后气体质量改变,当混合气体的质量不变时该反应达到平衡状态,故D不选;
故选A.
点评:本题考查化学平衡状态的判断,化学平衡状态的本质特征是正逆反应速率相等,注意只有反应前后改变的物理量才能作为判断依据,为易错点.

练习册系列答案
相关题目
如表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
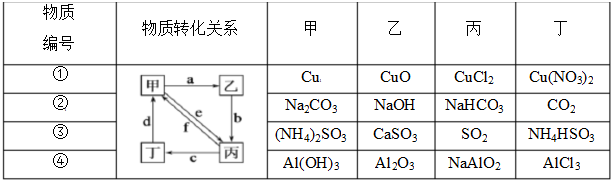

| A、②④ | B、①②③ |
| C、①③④ | D、①②③④ |
将足量二氧化硫通入下列各溶液中,所含离子因发生氧化还原反应而不能大量共存的是( )
| A、Na+、NH4+、Br-、Cl- |
| B、K+、Na+、SO42 -、SiO32 - |
| C、Na+、HCO3-、SO32 -、CH3COO- |
| D、H+、Fe3+、NO3-、SO32 - |
下列反应中属于氧化还原反应的是( )
| A、2NaHCO3=Na2CO3+CO2↑+H2O |
| B、2KMnO4=K2MnO4+MnO2+O2↑ |
| C、Ca(OH)2+CO2=CaCO3↓+H2O |
| D、Cu(OH)2+H2SO4=CuSO4+2H2O |
下列说法正确的是( )
| A、互为同位素的原子性质几乎完全相同 |
| B、丙氨酸CH3-CH(NH2)-COOH存在手性异构体 |
| C、标准状况下,相同体积的NH3、CH4、HF含有相同的电子数 |
| D、等体积的NO和O2混合后所得的混合气体的平均摩尔质量为41.33 g/mol |
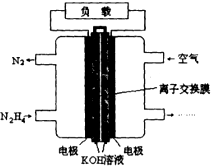 肼(N2H4)是火箭发射常用的燃料.一种以肼(N2H4)为燃料的电池装置如图所示. 该燃料电池的电极材料采用多孔导电材料,以提高电极反应物在电极表面的吸附量,并使它们与电解质溶液充分接触,以空气中的氧气作为氧化剂,KOH溶液作为电解质.
肼(N2H4)是火箭发射常用的燃料.一种以肼(N2H4)为燃料的电池装置如图所示. 该燃料电池的电极材料采用多孔导电材料,以提高电极反应物在电极表面的吸附量,并使它们与电解质溶液充分接触,以空气中的氧气作为氧化剂,KOH溶液作为电解质.