0 128761 128769 128775 128779 128785 128787 128791 128797 128799 128805 128811 128815 128817 128821 128827 128829 128835 128839 128841 128845 128847 128851 128853 128855 128856 128857 128859 128860 128861 128863 128865 128869 128871 128875 128877 128881 128887 128889 128895 128899 128901 128905 128911 128917 128919 128925 128929 128931 128937 128941 128947 128955 203614





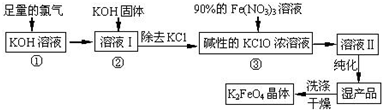






 的部分流程图:
的部分流程图:





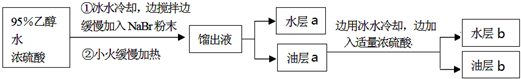
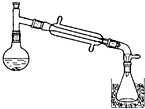 一溴乙烷为无色液体,熔点-119.1℃,沸点38.4℃,常用于汽油的乙基化、冷冻剂和麻醉剂.制备一溴乙烷的反应原理为:NaBr+H2SO4═HBr↑+NaHSO4,CH3CH2OH+HBr→CH3CH2Br+H2O.实验室可用如图装置制备一溴乙烷
一溴乙烷为无色液体,熔点-119.1℃,沸点38.4℃,常用于汽油的乙基化、冷冻剂和麻醉剂.制备一溴乙烷的反应原理为:NaBr+H2SO4═HBr↑+NaHSO4,CH3CH2OH+HBr→CH3CH2Br+H2O.实验室可用如图装置制备一溴乙烷