气体体积的大小,跟下列因素几乎无关的是( )
| A、物质的量 | B、温度 |
| C、压强 | D、气体分子直径 |
在3Cl2+8NH3=6NH4Cl+N2反应中,还原性最强的物质是( )
| A、Cl2 |
| B、NH3 |
| C、NH4Cl |
| D、N2 |
下列说法正确的是( )
| A、40gNaOH溶于1L水中所得溶液的物质的量浓度为1mol/L |
| B、不互溶的液态混合物可用分液的方法分离 |
| C、用砂纸打磨掉铝表面的氧化膜,在空气中点燃可像镁一样剧烈燃烧 |
| D、物质所含元素化合升高,一定是被另一种物质把它氧化了 |
200mL某硫酸盐溶液中,含硫酸根离子1.5NA个,含金属离子NA个,则该硫酸盐溶液的物质的量浓度为( )
| A、2.5 mol?L-1 |
| B、5 mol?L-1 |
| C、7.5 mol?L-1 |
| D、2 mol?L-1 |
下列说法不正确的是( )
| A、已知冰的熔化热为6.0kJ/mol,冰中氢键键能为20kJ/mol.假设每摩尔冰中有2 mol 氢键,且熔化热完全用于打破冰的氢键,则最多只能破坏冰中15%的氢键 |
| B、已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为α,Ka=(cα)2/[c(1-α)].若加入少量CH3COONa固体,则电离平衡CH3COOH?CH3COO-+H+向左移动,α减小,Ka减小 |
| C、由N2和H2合成1molNH3时可放出46.2kJ/mol的热量.已知N≡N键的键能是948.9kJ/mol,H-H键的键能是436.0kJ/mol,则N-H键的键能是 391.55kJ/mol |
| D、NH4HCO3(s)═NH3(g)+H2O(g)+CO2(g)△H=+185.57 kJ/mol,该反应能自发进行的原因是体系有自发地向混乱度增加的方向转变的倾向 |
设NA为阿佛加德罗常,下列叙述正确的是( )
| A、在100mL0.5mol/LCH3COOH溶液中CH3COOH分子数等于0.05NA |
| B、在标况下,22.4L辛烷含共价键数为25NA |
| C、已知PbI2的KSP=7.0×10-9,将1.0×10-2mol/L的KI与Pb(NO3)2溶液等体积混合,则生成PbI2沉淀所需Pb(NO3)2溶液的最小浓度为5.6×10-4 mol/L |
| D、15.6gNa2O2跟过量CO2反应时,转移电子数为2NA |
 实验小组中甲同学按图完成实验,发现电流计指针偏转,乙同学将图中盐桥(琼脂和饱和氯化钾)换成U形铜丝代替盐桥,发现电流计指针也发生偏转,以下说法正确的是( )
实验小组中甲同学按图完成实验,发现电流计指针偏转,乙同学将图中盐桥(琼脂和饱和氯化钾)换成U形铜丝代替盐桥,发现电流计指针也发生偏转,以下说法正确的是( )| A、甲同学实验过程中,ZnSO4溶液中阴离子总浓度不会发生改变 |
| B、甲同学实验过程中,Zn片被氧化,铜片被还原 |
| C、乙同学将盐桥换成铜丝后,导线中电流方向不会发生变化 |
| D、乙同学将盐桥换成铜丝后,U形铜丝的两端电极反应类型一致 |
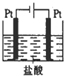
 用如图装置模拟人工肾脏的工作原理,电解生成的Cl2将尿素[CO(NH2)2]氧化成N2排出,则下列说法错误的是( )
用如图装置模拟人工肾脏的工作原理,电解生成的Cl2将尿素[CO(NH2)2]氧化成N2排出,则下列说法错误的是( )| A、电解结束后,阴极室溶液与电解前相比pH增大 |
| B、尿素被氧化的化学方程式为CO(NH2)2+3Cl2+H2O=N2+CO2+6HCl |
| C、电源的正极为b |
| D、电解结束后,若两极共收集到气体13.44 L(标准状况)时,则被氧化的尿素为7.2 g(忽略气体的溶解) |