题目内容
某电池工作时有如下特征:①、阳极质量不断减小;②、阴极表面有无色无味的气泡产生.则该电池可能为下列的( )
A、 |
B、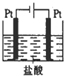 |
C、 |
D、 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A、A为电解池,阴极是银离子放电生成Ag;
B、B为电解池,阳极为惰性电极;
C、C为电解池阳极上铁放电生成亚铁离子,阴极氢离子放电生成氢气;
D、D为原电池,负极质量减小,正极生成氢气.
B、B为电解池,阳极为惰性电极;
C、C为电解池阳极上铁放电生成亚铁离子,阴极氢离子放电生成氢气;
D、D为原电池,负极质量减小,正极生成氢气.
解答:
解:A、阴极不能生成气体,故A错误;
B、阳极质量不变,故B错误;
C、C为电解池阳极上铁放电生成亚铁离子质量减小,阴极氢离子放电生成氢气为无色无味气体,故C正确;
D、D为原电池,有正负极无阴阳极,故D错误;
故选C.
B、阳极质量不变,故B错误;
C、C为电解池阳极上铁放电生成亚铁离子质量减小,阴极氢离子放电生成氢气为无色无味气体,故C正确;
D、D为原电池,有正负极无阴阳极,故D错误;
故选C.
点评:本题考查了电解池中电极产物的判断,注意电解池中电极上离子的放电顺序,题目难度中等.

练习册系列答案
相关题目
下列化学用语正确的是( )
A、聚丙烯的结构简式: |
B、甲醛的电子式: |
C、光气COCl2的结构式: |
| D、甲酸甲酯的实验式:C2H4O2 |
关于下列各装置图的叙述中,不正确的是( )

| A、用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液 |
| B、用装置①进行电镀,镀件接在b极上 |
| C、装置②的总反应是:Cu+2Fe3+═Cu2++2Fe2+ |
| D、装置③中的铁钉几乎没被腐蚀 |
在3Cl2+8NH3=6NH4Cl+N2反应中,还原性最强的物质是( )
| A、Cl2 |
| B、NH3 |
| C、NH4Cl |
| D、N2 |
某非金属元素的原子核外最外层电子数是次外层电子数的一半,该元素说法正确的是( )
| A、在自然界中只以化合态的形式存在 |
| B、单质常用作半导体材料和光导纤维 |
| C、最高价氧化物不与任何酸反应 |
| D、高温下其最高价氧化物与C反应生成该非金属单质和CO2 |
能正确表示下列反应的离子方程式是( )
| A、碳酸氢钠溶液与稀盐酸反应:CO32-+2H+=CO2↑+H2O |
| B、碳酸钡与醋酸反应:BaCO3+CH3COOH=Ba2++CH3COO-+CO2↑+H2O |
| C、把金属铁放入稀硫酸中:2Fe+6H+=2Fe3++3H2↑ |
| D、FeCl3溶液中加入过量氨水:Fe3++3NH?H2O=Fe(OH)3↓+3NH4+ |
