已知醋酸、醋酸根离子在溶液中存在下列平衡及其对应的平衡常数
CH3COOH?CH3COO-+H+ K1=1.75×10-5△H1>0
CH3COO-+H2O?CH3COOH+OH- K2=5.71×10-10△H2>0
常温下,将等体积、等物质的量浓度的醋酸和醋酸钠溶液混合,则下列叙述正确的是( )
CH3COOH?CH3COO-+H+ K1=1.75×10-5△H1>0
CH3COO-+H2O?CH3COOH+OH- K2=5.71×10-10△H2>0
常温下,将等体积、等物质的量浓度的醋酸和醋酸钠溶液混合,则下列叙述正确的是( )
| A、对混合溶液进行微热,K1增大、K2减小 |
| B、混合溶液的pH>7 |
| C、混合溶液中c(CH3COO-)>c(Na+) |
| D、温度不变,若在混合溶液中加入少量NaOH固体,则c(CH3COO-)减小 |
下列叙述正确的是( )
| A、将纯水加热,水的离子积变大、pH变小、溶液呈酸性 |
| B、pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,c(H+)相等 |
| C、CH3COONa溶液加水稀释后,恢复至原温度,pH和Kw均减小 |
| D、中和等体积和等pH的盐酸和醋酸溶液所消耗的NaOH物质的量相同 |
常温下,有 ①Na2CO3溶液 ②CH3COONa溶液 ③NaOH溶液各25mL,它们的物质的量浓度均为0.1mol?L-1,下列说法正确的是( )
| A、3种溶液pH的大小顺序是 ③>②>① |
| B、若将此3种溶液稀释相同倍数,pH变化最大的是② |
| C、若分别逐滴加入25mL 0.1 mol?L-1盐酸后,反应后所得溶液pH最大的是① |
| D、以上3种溶液中水的电离程度相同 |
某溶液中含有大量的下列离子:X离子、NH4+、Cl-和Al3+,经测定X离子、NH4+、Cl-和Al3+的物质的量浓度之比为2:1:5:2,则X离子可能是( )
| A、OH- |
| B、Na+ |
| C、NO3- |
| D、Ag+ |
在含有Fe3+、Fe2+、Al3+、Cl-的稀溶液中,加入足量的Na2O2固体,充分反应后再加入过量的稀盐酸,溶液中离子数目变化最小的是( )
| A、Al3+、Cl- |
| B、Al3+ |
| C、Fe2+、Cl- |
| D、Fe3+ |
电解饱和食盐水的装置如右图,通电一段时间后,下列说法一定正确的是( )


| A、滴加适量盐酸,可以使电解质溶液复原 |
| B、在U形管两端分别滴加酚酞试液,右端变红 |
| C、可用中和滴定的方法测定生成的氢氧化钠溶液的物质的量浓度 |
| D、若得到22.4 LH2(标准状况下),理论上需要转移NA个电子(NA为阿伏加德罗常数的值) |
以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Au等杂质)的电解精炼,下列说法正确的是( )
| A、利用阳极泥可回收Ag、Au等金属 |
| B、阳极减少的质量一定等于阴极增加的质量 |
| C、精炼过程中,CuSO4溶液的浓度不发生改变 |
| D、因部分电能转化为热能,精炼时通过的电量与阴极铜的析出量无确定关系 |
下列事实不能证明醋酸是弱酸的是( )
| A、醋酸钠溶液的pH>7 |
| B、常温下,0.1 mol?L-1醋酸溶液pH=2.5 |
| C、醋酸能使紫色石蕊试液变红 |
| D、pH=3的醋酸溶液稀释100倍后pH<5 |
如图是以石墨为电极,电解CuCl2溶液的装置图,下列说法正确的是( )
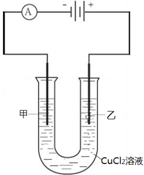

| A、甲电极为阳极 |
| B、阴极处能产生使湿润淀粉KI试纸变蓝的气体 |
| C、阴极发生还原反应 |
| D、通电时,溶液中的离子作定向运动 |