题目内容
如图是以石墨为电极,电解CuCl2溶液的装置图,下列说法正确的是( )
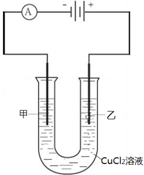

| A、甲电极为阳极 |
| B、阴极处能产生使湿润淀粉KI试纸变蓝的气体 |
| C、阴极发生还原反应 |
| D、通电时,溶液中的离子作定向运动 |
考点:电解原理
专题:
分析:A、根据甲与电源负极相连为阴极判断;
B、根据阴极是氧化性强的阳离子铜离子先放电析出金属铜判断;
C、阴极是氧化性强的阳离子铜离子先放电析出金属铜发生还原反应;
D、通电时,阴离子移向阳极,阳离子移向阴极;
B、根据阴极是氧化性强的阳离子铜离子先放电析出金属铜判断;
C、阴极是氧化性强的阳离子铜离子先放电析出金属铜发生还原反应;
D、通电时,阴离子移向阳极,阳离子移向阴极;
解答:
解:A、甲与电源负极相连为阴极,故A错误;
B、电解过程中在阴极是氧化性强的阳离子铜离子先放电析出金属铜,故B错误;
C、阴极是氧化性强的阳离子铜离子先放电析出金属铜发生还原反应,故C正确;
D、通电时,阴离子移向阳极,阳离子移向阴极,所以溶液中的离子作定向运动,故D正确.
故选CD.
B、电解过程中在阴极是氧化性强的阳离子铜离子先放电析出金属铜,故B错误;
C、阴极是氧化性强的阳离子铜离子先放电析出金属铜发生还原反应,故C正确;
D、通电时,阴离子移向阳极,阳离子移向阴极,所以溶液中的离子作定向运动,故D正确.
故选CD.
点评:本题是一道电解原理知识的题目,要熟记电解池的工作原理,学以致用.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
 如图是某有机物分子的比例模型,黑色的是碳原子,白色的是氢原子,灰色的是氧原子.则该物质不具有的性质是( )
如图是某有机物分子的比例模型,黑色的是碳原子,白色的是氢原子,灰色的是氧原子.则该物质不具有的性质是( )| A、使紫色石蕊变红 |
| B、与钠反应 |
| C、发生酯化反应 |
| D、发生氧化反应 |
铁是人类应用较早,当前应用量最大的金属元素.下列有关铁及其化合物的有关说法中正确的是( )
| A、Fe3+与KSCN产生血红色沉淀 |
| B、赤铁矿的主要成分是Fe3O4 |
| C、除去FeCl2溶液中的FeCl3杂质可以向溶液中加入铁粉,然后过滤 |
| D、铁与水蒸气在高温下的反应产物为Fe2O3和H2 |
用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A、在标准状况下,11.2 L H2O中含有的分子数为0.5 NA |
| B、32 g O2所含的原子数为2 NA |
| C、1 mol/L NaCl溶液中含有的Na+的数为NA |
| D、1 mol Na2O2中离子总数为4 NA |
下列生活中的做法不恰当的是( )
| A、贮氯罐意外泄漏,应沿逆风方向疏散群众 |
| B、铝制餐具不宜长期存放酸性、碱性或咸的食物 |
| C、氢氧化铝可作胃酸的中和剂 |
| D、漂白粉能在空气中长期存放 |
某溶液中含有大量的下列离子:X离子、NH4+、Cl-和Al3+,经测定X离子、NH4+、Cl-和Al3+的物质的量浓度之比为2:1:5:2,则X离子可能是( )
| A、OH- |
| B、Na+ |
| C、NO3- |
| D、Ag+ |
 某温度下,相同pH值的氨水和氢氧化钠溶液分别加水稀释,平衡pH值随溶液体积变化的曲线如图所示.据图判断正确的是( )
某温度下,相同pH值的氨水和氢氧化钠溶液分别加水稀释,平衡pH值随溶液体积变化的曲线如图所示.据图判断正确的是( )| A、Ⅱ为氨水稀释时的pH值变化曲线 |
| B、a、b、c三点溶液的导电性:c>b=a |
| C、a、b、c三点溶液中水的电离程度:c=b>a |
| D、用相同浓度的盐酸分别与等体积的b、c处溶液恰好完全反应,消耗盐酸的体积:Vb=Vc |
25℃时,0.01mol/L的稀盐酸溶液中水电离出的H+的浓度是( )
| A、5×10-13mol/L |
| B、0.01 mol/L |
| C、1×10-7 mol/L |
| D、1×10-12mol/L |
 是一种新型可生物降解的高分子材料,主要用于制造可降解纤维,可降解塑料和医用材料.它以淀粉为原料,先水解为葡萄糖,再在乳酸菌的作用下降葡萄糖转变为乳酸
是一种新型可生物降解的高分子材料,主要用于制造可降解纤维,可降解塑料和医用材料.它以淀粉为原料,先水解为葡萄糖,再在乳酸菌的作用下降葡萄糖转变为乳酸 ,乳酸在催化剂的催化下聚合成聚乳酸.聚乳酸材料废弃后,先水解成乳酸,乳酸在微生物的作用下分解为CO2和H2O.请用化学方程式表示上述聚合与降解的过程.
,乳酸在催化剂的催化下聚合成聚乳酸.聚乳酸材料废弃后,先水解成乳酸,乳酸在微生物的作用下分解为CO2和H2O.请用化学方程式表示上述聚合与降解的过程.