相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:X2(g)+3Y2(g)?2XY3(g)△H=-92.6kJ.mol-1实验测得反应在起始、达到平衡时的有关数据如下表所示:下列叙述不正确的是( )
| 容器编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| X2 | Y2 | XY3 | ||
| ① | 1 | 3 | 0 | 放热23.15kJ |
| ② | 0.6 | 1.8 | 0.8 | Q(Q>0) |
| A、容器①、②中反应的平衡常数相等 |
| B、达平衡时,两个容器中XY3的物质的量浓度均为2mol?L-1 |
| C、容器②中反应达到平衡时放出的热量为Q |
| D、若将容器①体积缩小为0.20L,则达平衡时放出的热量大于23.15kJ |
下列叙述中,正确的是( )
A、稀释Na2CO3溶液时,
| ||||||
B、500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应,放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)
| ||||||
| C、相同条件下,2mol氢原子所具有的能量小于1mol氢分子所具有的能量 | ||||||
| D、常温下反应4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s)的△H<0,△S<0 |
下列溶液加热蒸干后并灼烧,能析出溶质固体的是( )
| A、AlCl3 |
| B、KHCO3 |
| C、Fe2(SO4)3 |
| D、NH4HCO3 |
相同物质的量浓度的NaCN和NaClO相比,NaCN溶液的pH较大,则同温同体积同浓度的HCN和HC1O说法正确的是( )
| A、电离程度:HCN>HClO |
| B、pH:HClO>HCN |
| C、NaOH恰好完全反应时,消耗NaOH的物质的量:HClO>HCN |
| D、酸根离子浓度:c(ClO-)>c(CN--) |
下列离子方程式中,属于水解反应的是( )
| A、HCOOH+H2O═HCOO-+H3O+ |
| B、CO2+H2O═HCO3-+H+ |
| C、CO32-+H2O═HCO3-+OH- |
| D、HS-═S2-+H+ |
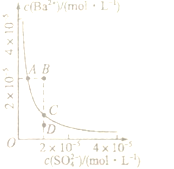 某温度下,BaSO4在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是( )
某温度下,BaSO4在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是( )| A、加入Na2SO4可以使溶液由A点变到B点 |
| B、通过蒸发可以使溶液由D点变到C点 |
| C、D点无BaSO4沉淀生成 |
| D、A点对应的Ksp等于c点对应的Ksp |
 钠及其化合物具有广泛的用途.
钠及其化合物具有广泛的用途.
