设阿伏加德罗常数为NA,则下列说法正确的是( )
| A、15g甲基(-CH3)所含有的电子数是9NA |
| B、常温常压下,0.1mol甲烷与甲醛混合气体中所含碳原子数为0.1NA |
| C、标准状况下,1L庚烷充分燃烧后生成的气态产物的分子数为7/22.4 NA |
| D、常温常压下,1mol苯分子中含有碳碳双键数为3NA |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、2.24LH2含有的原子数为0.2NA |
| B、常温常压下,18gNH4+的电子数为10 NA |
| C、标准状况下,1NAH2O分子占有的体积约为22.4L |
| D、0.5 mol/L的AlCl3溶液中,Cl-的数目为1.5NA |
下列叙述中正确的是( )
| A、常温常压下,1 mol羟基(-OH)所含的电子数为10 NA |
| B、由Cu、Zn和稀硫酸组成的原电池工作时,若Cu极生成0.2 g H2,则电路中通过0.2 mol电子 |
| C、在标准状况下,11.2 L NO与11.2 L 02混合后气体分子数为0.75 NA |
| D、l mol Na202,与足量水反应,转移电子的物质的量为2 mol |
N、O、S、Si是重要的非金属元素,下列说法正确的是( )
| A、N、O、S、Si的原子半径逐渐增大,非金属性逐渐减弱 |
| B、SO2和SiO2既能与NaOH溶液反应,又能与某些酸反应 |
| C、N、S的氧化物既是形成光化学烟雾,又是形成酸雨的主要物质 |
| D、N、Si、S的单质均能和氧气反应,且产物分别是NO2、SiO2和SO2 |
有一种AB2C2型分子,在该分子中以A为中心原子,下列关于它的分子构型和有关同分异构体的各种说法正确的是( )
| A、假如为平面四边形,则有两种同分异构体; |
| B、假如为四面体,则有二种同分异构体; |
| C、假如为平面四边形,则无同分异构体 |
| D、假如为四面体,则无同分异构体. |
设NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A、1 mol Na2O2跟 H2O反应转移电子的数目为2NA |
| B、27g铝跟NaOH溶液反应转移电子的数目为3NA |
| C、常温常压下,22.4 L氯气所含原子数为2NA |
| D、标准状况下,22.4 L蒸馏水所含分子数为NA |
已知NaOH+H2O2=H2O+NaHO2.现用H2O2-Al燃料电池电解尿素[CO(NH2)2]和KOH的混合溶液制备氢气 (c、d均为惰性电极,电解池中隔膜仅阻止气体通过).下来说法不正确的是( )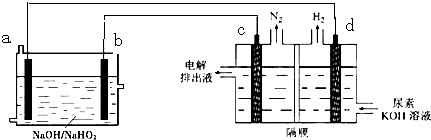

| A、燃料电池总反应为:3HO2-+2Al=OH-+2AlO2-+H2O |
| B、电极b是正极,且反应后该电极区pH增大 |
| C、每消耗27g Al,理论上产生11.2L(标准状况下)氮气 |
| D、反应时,电子的流向为:a→b→c→d. |
下列装置的线路接通后,经过一段时间,溶液的pH值明显下降的是( )
A、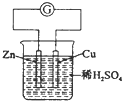 |
B、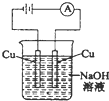 |
C、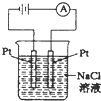 |
D、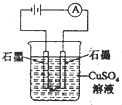 |
下列各组离子在溶液中能够大量共存,当溶液中c(H+)=10-1mol.L-1,能产生气体,而当溶液中c(H+)=10-13mol.L-1,能产生沉淀,则该组离子可能是( )
| A、Fe2+、Na+、SO42-、NO3- |
| B、NO3-、Ca2+、H+、HCO3- |
| C、Cu2+、NH4+、SO42-、Cl- |
| D、Ba2+、K+、Cl-、NO3- |
 按要求书写下列热化学方程式
按要求书写下列热化学方程式