题目内容
已知NaOH+H2O2=H2O+NaHO2.现用H2O2-Al燃料电池电解尿素[CO(NH2)2]和KOH的混合溶液制备氢气 (c、d均为惰性电极,电解池中隔膜仅阻止气体通过).下来说法不正确的是( )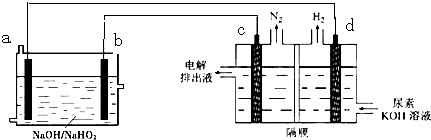

| A、燃料电池总反应为:3HO2-+2Al=OH-+2AlO2-+H2O |
| B、电极b是正极,且反应后该电极区pH增大 |
| C、每消耗27g Al,理论上产生11.2L(标准状况下)氮气 |
| D、反应时,电子的流向为:a→b→c→d. |
考点:原电池和电解池的工作原理
专题:
分析:电解时,电池反应时中,氮元素化合价由-3价变为0价,H元素化合价由+1价变为0价,所以生成氮气的电极是阳极,生成氢气的电极是阴极,则a是负极、b为正极,
H2O2-Al燃料电池工作时,Al为负极被氧化,H2O2为正极被还原,以此解答该题.
H2O2-Al燃料电池工作时,Al为负极被氧化,H2O2为正极被还原,以此解答该题.
解答:
解:A.H2O2-Al电池中电解池溶液呈碱性,HO2-被还原生成水,Al被氧化生成AlO2-,电池总反应为3HO2-+2Al=OH-+2AlO2-+H2O,故A正确;
B.c生成氮气,说明尿素被氧化,则b为正极,正极方程式为3HO2-+6e-+3H2O=9OH-,反应后该电极区pH增大,故B正确;
C.每消耗27g Al,则转移3mol电子,电解池阳极中氮元素化合价由-3价变为0价,在可生成0.5mol氮气,理论上产生气体体积为11.2L(标准状况下),故C正确;
D.电子从原电池负极→电解池阴极,从电解池阳极→原电池正极,即a→d,c→b.故D错误.
故选D.
B.c生成氮气,说明尿素被氧化,则b为正极,正极方程式为3HO2-+6e-+3H2O=9OH-,反应后该电极区pH增大,故B正确;
C.每消耗27g Al,则转移3mol电子,电解池阳极中氮元素化合价由-3价变为0价,在可生成0.5mol氮气,理论上产生气体体积为11.2L(标准状况下),故C正确;
D.电子从原电池负极→电解池阴极,从电解池阳极→原电池正极,即a→d,c→b.故D错误.
故选D.
点评:本题综合考查原电池以及电解原理,为高频考点,侧重于学生的分析能力的考查,明确元素化合价变化是解本题关键,根据元素化合价变化与阴阳极的关系来分析解答,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、2.24LH2含有的原子数为0.2NA |
| B、常温常压下,18gNH4+的电子数为10 NA |
| C、标准状况下,1NAH2O分子占有的体积约为22.4L |
| D、0.5 mol/L的AlCl3溶液中,Cl-的数目为1.5NA |
设NA 为阿伏加德罗常数的值.下列说法正确的是( )
| A、室温下,1LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA |
| B、0.1molMg在空气中完全燃烧生成MgO和Mg3N2,转移的电子数为0.2NA |
| C、标准状况下,22.4 L Cl2溶于足量NaOH溶液中,转移的电子数目为0.2NA |
| D、1 L 0.1 mol?L-1的Fe2(SO4)3溶液中,Fe3+的数目为0.2NA |
下列物质的俗名、化学式、主要用途都正确的是( )
| A、生石膏(2CaSO4?H2O):用于制造各种模型 |
| B、纯碱(NaHCO3):用于制玻璃、肥皂、纺织 |
| C、硫酸钡(BaSO4):作白色颜料、“钡餐” |
| D、胆矾(CuSO4):用于制造农药 |


 )出发,可发生图示的一系列反应,图中化合物D能使FeCl3溶液显紫色,G能进行银镜反应.E和H常温下为气体.试回答:
)出发,可发生图示的一系列反应,图中化合物D能使FeCl3溶液显紫色,G能进行银镜反应.E和H常温下为气体.试回答: