将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2,即构成甲烷燃料电池.已知通入CH4的一极,其电极反应式是:CH4+10OH--8e-=CO32-+7H2O;通入O2的另一极,其电极反应式是:O2+2H2O+4e-=4OH-,下列叙述不正确的是( )
| A、通入CH4的电极为负极 |
| B、正极发生还原反应 |
| C、此电池工作时溶液中阴离子向正极移动 |
| D、该电池使用一段时间后应补充KOH |
关于铜锌原电池的叙述,正确的是( )
| A、铜是负极,铜片上有气泡产生 |
| B、铜片质量逐渐减少 |
| C、电流从锌片经导线流向铜片 |
| D、氢离子在铜片表面被还原后生成H2 |
下列说法中,不正确的是( )
| A、若反应中形成化学键释放的能量大于断裂化学键所吸收的能量,则是放热反应 |
| B、若反应物的能量大于生成物的能量,则是放热反应 |
| C、化学反应中能量变化的大小与反应物的质量多少无关 |
| D、化学反应必然伴随着能量的变化和化学键的变化 |
下列装置能构成原电池的是( )
A、 酒精 |
B、 AgNO3溶液 |
C、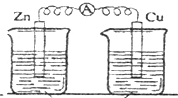 稀H2SO4 |
D、 稀H2SO4 |
以下是摘自高二实验班某学生在这次期中考试复习中对教材必修3第一章《原子结构》的总结,其中与教材说法不符的是( )
| A、同一原子的能层越高,s电子云半径越大 |
| B、任一能层的能级总是从s能级开始,而且能级数等于该能层序数 |
| C、书写电子排布式时,按照构造原理,依据电子的填充顺序从左到右书写能级 |
| D、处于最低能量的原子叫做基态原子,我们通常所说的电子排布指的是基态原子的电子排布 |
如图各烧杯中盛有海水,铁在其中被腐蚀时由快到慢的顺序是( )

| A、④>②>①>③ |
| B、②>①>③>④ |
| C、④>②>③>① |
| D、③>②>④>① |
下列分子中所有原子都满足最外层为8个电子结构的是( )
| A、BF3 |
| B、PCl5 |
| C、H2O |
| D、CCl4 |
氢氧燃料电池是一种高效、环境友好的发电装置,它是以铂作电极,KOH溶液作电解液,总反应为:2H2+O2=2H2O,正极反应为:O2+2H2O+4e-=4OH- 下列叙述不正确的是( )
| A、H2通入负极区 |
| B、O2通入正极区 |
| C、负极发生氧化反应 |
| D、正极发生氧化反应 |

