已知氢氟酸酸性强于氢氰酸(HCN),下列判断正确的是( )
| A、NaCN 与 HCN 的混合液中一定有 C(Na+)>C(CN-)>C(OH-)>C(H+) |
| B、氢氟酸溶液的导电性一定强于氢氰酸 |
| C、相同温度下,同浓度、同体积的NaF溶液和NaCN溶液,离子数目前者大于后者 |
| D、氢氟酸能与Na2C03反应生成C02气体,HCN也一定能与Na2C03反应生成C02气体 |
下列关于实验的说法正确的是( )
| A、将二氧化碳通人硅酸钠溶液以证明碳酸的酸性比硅酸强 |
B、如图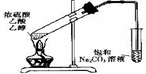 装置中,导管不能伸人液面的原因是产物易溶于水 装置中,导管不能伸人液面的原因是产物易溶于水 |
| C、用碱石灰可干燥氯气 |
| D、用普通玻璃棒蘸取溶液做焰色反应以证明溶液含有Na十 |
下列说法正确的是( )
| A、向1 mo1?L-l CH3COOH溶液中加入少量CH3COONa固体,由于CH3COONa水解显碱性,所以溶液的pH升高 | ||||||||||
B、25℃时,将a mo1?L-l氨水与0.01 moI?L-1盐酸等体积混合,反应完全时溶液中Kb=
| ||||||||||
C、根据下表数据可以计算出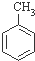 (g)+3H2(g)→ (g)+3H2(g)→ (g)的焓变 (g)的焓变
| ||||||||||
| D、已知298K时,MgCO3的Ksp=6.82×10-6,溶液中c(Mg2+)=0.0001 mol?L-1,c(CO32-)=0.0001 mol?L-1,此时Mg2+和CO32-不能共存 |
已知浓度商(Qc)表示任意状态下反应体系中物质的浓度关系,其表达式与化学平衡常数的表达式相同.保持温度和体积不变,可逆反应:A(s)+2B(g)?2C(g)+D(g)△H<0,在甲、乙、丙三个容器中建立平衡的相关信息如下表.则下列说法正确的是( )
| 容器 | 体积 | 起始物质 | 平衡时C的 物质的量 | 平衡时B的 体积分数 | 平衡常数 |
| 甲 | 1L | 1molA+2molB | 1mol | φ甲 | K甲 |
| 乙 | 1L | 4molC+2molD | n1mol | φ乙 | K乙 |
| 丙 | 2L | 4molC+2molD | n2mol | φ丙 | K丙 |
| A、在建立平衡的过程中,甲的Qc逐渐减小,乙和丙的Qc逐渐增大 |
| B、K甲=K丙>K乙 |
| C、升高甲的温度,可使φ甲=φ乙 |
| D、n1=1.6,n2=2 |


 A、B、C、D、E、F为前四周期原子序数依次增大的非稀有气体元素.其中:A的一种单质是自然界最硬的物质;B与A同周期且基态原子中s能级与p能级上的电子数相等;C于B同主族;D为同周期电负性最大的元素;E为使用最为广泛的金属;F的基态原子中没有单电子.请回答下列有关问题:
A、B、C、D、E、F为前四周期原子序数依次增大的非稀有气体元素.其中:A的一种单质是自然界最硬的物质;B与A同周期且基态原子中s能级与p能级上的电子数相等;C于B同主族;D为同周期电负性最大的元素;E为使用最为广泛的金属;F的基态原子中没有单电子.请回答下列有关问题: A、B、C、D、E、F是原子序数依次递增的前四周期元素.A是宇宙中含量最丰富的元素;D与E同主族,且E的原子序数是D的两倍;B与D组成的化合物是一种温室气体;C元素原子最外层P能级比S能级多1个电子;F原子的最外层电子数与A相同,其余各层均充满.据此回答下列问题.
A、B、C、D、E、F是原子序数依次递增的前四周期元素.A是宇宙中含量最丰富的元素;D与E同主族,且E的原子序数是D的两倍;B与D组成的化合物是一种温室气体;C元素原子最外层P能级比S能级多1个电子;F原子的最外层电子数与A相同,其余各层均充满.据此回答下列问题.