��Ŀ����
����˵����ȷ���ǣ�������
| A����1 mo1?L-l CH3COOH��Һ�м�������CH3COONa���壬����CH3COONaˮ���Լ��ԣ�������Һ��pH���� | ||||||||||
B��25��ʱ����a mo1?L-l��ˮ��0.01 moI?L-1����������ϣ���Ӧ��ȫʱ��Һ��Kb=
| ||||||||||
C�������±����ݿ��Լ����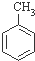 ��g��+3H2��g���� ��g��+3H2��g���� ��g�����ʱ� ��g�����ʱ�
| ||||||||||
| D����֪298Kʱ��MgCO3��Ksp=6.82��10-6����Һ��c��Mg2+��=0.0001 mol?L-1��c��CO32-��=0.0001 mol?L-1����ʱMg2+��CO32-���ܹ��� |
���㣺���������ˮ��Һ�еĵ���ƽ��,�йط�Ӧ�ȵļ���,�����ʱ�Ķ����жϼ��й�ph�ļ���,���ӹ�������
ר�⣺
������A����CH3COOH��Һ�м�������CH3COONa���壬��Һ�д��������Ũ���������ƴ�����룻
B������Һ��c��NH4+��=c��C1-����˵����Һ�����ԣ���c��H+��=c��OH-��=10-7��NH3?H2O�ĵ���ƽ�ⳣ��Kb=
��
C��������̼̼���ǽ���̼̼������̼̼˫��֮����������������̼̼˫����
D�������Һ��c��Mg2+��?c��CO32-����Ksp=6.82��10-6��������ܹ��棬�����ܹ��森
B������Һ��c��NH4+��=c��C1-����˵����Һ�����ԣ���c��H+��=c��OH-��=10-7��NH3?H2O�ĵ���ƽ�ⳣ��Kb=
| c(NH4+)c(OH-) |
| c(NH3?H2O) |
C��������̼̼���ǽ���̼̼������̼̼˫��֮����������������̼̼˫����
D�������Һ��c��Mg2+��?c��CO32-����Ksp=6.82��10-6��������ܹ��棬�����ܹ��森
���
�⣺A��CH3COOH�д��ڵ���ƽ��CH3COOH?H++CH3COO-����������ƣ�CH3COO-�����ӣ�������CH3COOH�ĵ��룬������Һ��c��H+����С������Һ��pH���ߣ���A����
B������Һ��c��NH4+��=c��C1-����˵����Һ�����ԣ���c��H+��=c��OH-��=10-7����NH3?H2O�ĵ���ƽ�ⳣ��Kb=
=
=
����B��ȷ��
C�������е�̼̼���ǽ��ڵ�����˫��֮����������������δ�����������ֵ���ʲ��ܼ�����÷�Ӧ���ʱ䣬��C����
D��c��Mg2+��?c��CO32-��=��0.0001��2=1��10-8��6.82��10-6�����Դ�ʱMg2+��CO32-�ܹ��棬��D����
��ѡB��
B������Һ��c��NH4+��=c��C1-����˵����Һ�����ԣ���c��H+��=c��OH-��=10-7����NH3?H2O�ĵ���ƽ�ⳣ��Kb=
| c(NH4+)c(OH-) |
| c(NH3?H2O) |
| 0.005��10-7 |
| 0.5��(a-0.01) |
| 10-9 |
| a-0.01 |
C�������е�̼̼���ǽ��ڵ�����˫��֮����������������δ�����������ֵ���ʲ��ܼ�����÷�Ӧ���ʱ䣬��C����
D��c��Mg2+��?c��CO32-��=��0.0001��2=1��10-8��6.82��10-6�����Դ�ʱMg2+��CO32-�ܹ��棬��D����
��ѡB��
���������⿼����ۺϣ�Ϊ�߿��������ͣ��漰��������ܽ�ƽ�⡢������ʵĵ��롢�ʱ��֪ʶ�㣬�����ܶȻ�������Ũ�Ȼ�֮��Ĺ�ϵ��������ʵĵ����ص㡢���ʵĽṹ��֪ʶ������������ѵ���Bѡ�ע�����Ϻ���Һ�������һ������ҺŨ�Ƚ�Ϊԭ����һ�룬��Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
�����Ŀ
 ��������ͪ�Ǻϳ�ij�ֿ���ҩ����Ҫ�м��壬��ṹ��ͼ��ʾ�����й��ڰ�������ͪ�����ʵ�������ȷ���ǣ�������
��������ͪ�Ǻϳ�ij�ֿ���ҩ����Ҫ�м��壬��ṹ��ͼ��ʾ�����й��ڰ�������ͪ�����ʵ�������ȷ���ǣ�������| A����������ͪ�ķ���ʽΪC22H22O8 |
| B�������к���4������̼ԭ�� |
| C���÷���һ���������ܷ����ӳɡ�ȡ������������ȥ��Ӧ |
| D��1mol������������3molNaOH��Ӧ |
�������и�ͼ���߱�������Ϣ���ó��Ľ��۲���ȷ���ǣ�������


| A��ͼ1��ʾ�����������Ϊ10 mL 0.1 mol?L-1NaOH��Һ����μ���0.1 mol?L-1 CH3COOH��Һ����Һ��pH�仯���ߣ���b�㴦�У�c��CH3COOH��+c��H+��=c��OH-�� |
| B��ͼ2��ʾ��ˮϡ��pH��ͬ������ʹ���ʱ��Һ��pH�仯���ߣ����Т��ʾ���ᣬ���ʾ���ᣬ����Һ�����ԣ�c��b��a |
| C��ͼ3��ʾH2��O2������Ӧ�����е������仯��H2��ȼ����Ϊ285.8 kJ?mol-1 |
| D����ͼ4�ó�����ȥCuSO4��Һ�е�Fe3+���ɲ�������Һ�м�������CuO��������Һ��pH��4���� |
���й����л����˵����ȷ���ǣ�������
| A�����ࡢ��֬��������һ�����ܷ���ˮ�ⷴӦ |
| B�������Cl2�ķ�Ӧ����ϩ��Br2�ķ�Ӧ����ͬһ���͵ķ�Ӧ |
| C��һ�������£�������1mol����1mol�ױ�������3molH2��Ӧ |
| D���Ҵ������������NaOHϡ��Һ��Ӧ����Ϊ�����о����й����š�-OH�� |
����ʵ����ȷ���ǣ�������
A�� �������ᾧ��Ũ�� |
B�� ���װ�������� |
C�� ̼���������ȷֽ� |
D�� ����е㲻ͬ�һ��ܵ�Һ������ |
ʵ���ҿ���ͼ��ʾװ�ø���ռ�ij����R�������ն����R����R�ǣ�������


| A��O2 |
| B��HCl |
| C��Cl2 |
| D��NH3 |



