常用的电池是一个液体电解质将两个固体电极隔开.而钠-硫(Na/S8)电池正相反,它是由固体电解质将两个液体电极隔开(如图),一个由钠-β-氧化铝固体电解质做成的中心管,将内室的熔融钠(熔点98℃)和外室的熔融硫(熔点119℃)隔开,并允许Na+通过.下列有关说法不正确的是( )
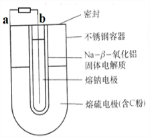

| A、a为电池的正极 |
| B、充电时b接电源的正极 |
| C、正极反应为:nS8+16ne-=8Sn2- |
| D、Na+可以穿过固体电解质和硫反应从而传递电流 |
形成原电池的条件一般有:①电解质溶液②两个电极③能自发地发生氧化还原反应④形成闭合回路
请根据上述条件判断下列装置中属于原电池的是( )
请根据上述条件判断下列装置中属于原电池的是( )
A、 NaCl溶液 |
B、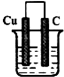 HCl溶液 |
C、 CuSO4溶液 |
D、 蔗糖溶液 |
锂空气电池放电时的工作原理如图所示.下列叙述正确的是( )


| A、放电时Li+由B极向A极移动 |
| B、电池放电反应为4Li+O2+2H2O=4LiOH |
| C、正极反应式为O2+4H++4e-=2H2O |
| D、电解液a可以为LiCl溶液 |
向VmLFeBr2溶液中缓慢通入amolCl2,结果溶液中有50% 的Br-被氧化为溴单质,则原FeBr2溶液的物质的量浓度为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列说法不正确的是( )
| A、催化剂可以改变化学反应速率 |
| B、2molSO2与lmolO2混合一定能生成2molSO3 |
| C、食物放在冰箱中会减慢食物变质的速率 |
| D、化学反应达到反应限度时,正反应的速率与逆反应的速率相等 |
已知C+CO2?2CO,正反应是吸热反应,反应速率为v1;N2+3H2?2NH3,正反应是放热反应,反应速率为v2.对于上述反应,当温度升高时,v1和v2的变化情况为( )
| A、都增大 |
| B、都减小 |
| C、v1增大,v2减小 |
| D、v1减小,v2增大 |
下列有关说法正确的是( )
| A、在潮湿的环境中,铜容易发生析氢腐蚀形成铜绿 |
| B、常温下,pH均为5的盐酸、氯化铵溶液中,水的电离程度相同 |
| C、8NH3(g)+6NO(g)═7N2(g)+12H2O(g)△H<0,则该反应一定能自发进行 |
| D、对于乙酸乙酯的水解反应(△H>0),加入少量氢氧化钠溶液并加热,该反应的反应速率和平衡常数均增大 |
已知4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H<0,下列有关叙述正确的( )
| A、上述反应的化学反应速率关系:2 v(NH3)=3 v(H2O) |
| B、若在2L的密闭容器中反应,经过3min后NH3的物质的量由10mol变为7mol 则v (NH3)=0.5mol?L-1?s-1 |
| C、达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大 |
| D、若降低温度,反应速率将会减小且平衡将被破坏 |

 有人设想以N2和H2为反应物,以溶有A物质的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如右图所示,
有人设想以N2和H2为反应物,以溶有A物质的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如右图所示,