如图为不同温度下水的电离平衡曲线,巳知pOH=-lgc(OH -),下列说法正确的是( )


| A、T1和T2的关系是:T1>T2 |
| B、Kw的关系是:B>C>A=D=E |
| C、A点到D点:加入少量酸可实现 |
| D、T2时:pH=2的硫酸与pH=12的NaOH溶液等体枳混合,溶液呈中性 |
室温下向10mL pH=3的醋酸溶液中加水稀释后,下对说法正确的是( )
| A、溶液中导电粒子的数目减少? | ||
| B、醋酸的电离程度增大,c(H+)亦增大 | ||
C、溶液中
| ||
| D、再加入10 mL pH=ll的NaOH溶液,混合液的PH=7 |
化学与生活密切相关,下列说法正确的是( )
| A、明矾可用于水的消毒,杀菌 |
| B、生石灰、铁粉,硅胶是食品包装中常用的干燥剂 |
| C、福尔马林可作食品的保鲜剂 |
| D、二氧化硅可用于制造光导纤维 |
下列说法正确的是( )
| A、常温下向饱和AgCl水溶液中加入盐酸,Ksp值变大 |
| B、用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小 |
| C、在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大 |
| D、物质的溶解度随温度的升高而增加,物质的溶解都是吸热的 |
将足量的AgCl(s)分别添加到下述四种溶液中,所得溶液c(Ag+)最小的是( )
| A、10 mL 0.4mol/L的盐酸 |
| B、10 mL 0.3mol/L MgCl2溶液 |
| C、10 mL 0.5mol/LNaCl溶液 |
| D、10 mL 0.1mol/L AlCl3溶液 |
用铂作电极电解1000mL 0.1mol/L AgNO3溶液,通电一段时间后关闭电源,测得溶液的质量减少了13.4g.下列有关叙述正确的是(NA代表阿伏加德罗常数的值)( )
| A、电解过程中流经外电路的电子数目为0.1NA |
| B、在标准状况下,两极共产生3.92L气体 |
| C、电解后溶液的pH为2(假设溶液体积不变) |
| D、加入13.8g Ag2CO3可将溶液彻底复原 |
已知:Ksp(AgCl)=1.56×10-10,Ksp(AgI)=1.56×10-16,Ksp(Ag2CrO4)=2.0×10-12.下列有关说法正确的是( )
| A、相同温度下,饱和溶液中的Ag+浓度:AgCl>Ag2CrO4>AgI |
| B、向饱和食盐水中加AgNO3,形成AgCl沉淀时,溶液中的Ag+浓度为1.34×10-5 mol?L-1 |
| C、向含AgI难溶物的溶液中,逐滴加入饱和食盐水,原难溶物会变成白色 |
| D、向含Cl-、I-和CrO42-浓度均为0.010 mol?L-1的溶液中,逐滴加入AgNO3溶液,最先形成Ag2CrO4沉淀 |
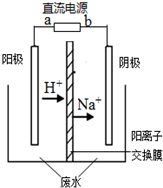 最近有研究人员利用隔膜电解法处理高浓度的乙醛废水.乙醛分别在阴、阳极发生反应,转化为乙醇和乙酸.实验室以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示.下列说法不正确的是( )
最近有研究人员利用隔膜电解法处理高浓度的乙醛废水.乙醛分别在阴、阳极发生反应,转化为乙醇和乙酸.实验室以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示.下列说法不正确的是( )| A、电解过程中,阴极附近的乙醛被氧化 |
| B、阳极反应CH3CHO-2e-+H2O═CH3COOH+2H+ |
| C、若以CH4-空气燃料电池为直流电源,燃料电池的b极应通入CH4 |
| D、现处理含1mol乙醛的废水,至少需转移1mol电子 |
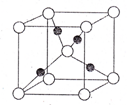 A、B、C、D、E为前四周期中原子序数依次增大的元素,相关的信息如下:
A、B、C、D、E为前四周期中原子序数依次增大的元素,相关的信息如下: 前四周期原子序数依次增大的X、Y、Z、Q、E五种元素中,X元素原子核外有三种不同的能级且各个能级所填充的电子数相同,Z是地壳内含量(质量分数)最高的元素,Q原子核外的M层中只有两对成对电子,E+核外各能层电子均已充满.请回答下列问题:
前四周期原子序数依次增大的X、Y、Z、Q、E五种元素中,X元素原子核外有三种不同的能级且各个能级所填充的电子数相同,Z是地壳内含量(质量分数)最高的元素,Q原子核外的M层中只有两对成对电子,E+核外各能层电子均已充满.请回答下列问题: